题目内容
4.用微粒的相关知识解释下列现象,正确的是( )| A. | 缉毒犬能根据气味发现毒品,是由于分子在不断运动 | |
| B. | 変瘪的乒乓球放入热水中能鼓起来,是由于分子受热变大 | |
| C. | 铝制品中的铝原子是静止不动的 | |
| D. | 将石块研磨成粉状,说明分子变小了 |
分析 根据分子的基本特征:分子质量和体积都很小;分子之间有间隔;分子是在不断运动的;同种的分子性质相同,不同种的分子性质不同,可以简记为:“两小运间,同同不不”,结合事实进行分析判断即可.
解答 解:A、缉毒犬能根据气味发现毒品,是因为毒品中含有的分子是在不断运动的,向四周扩散,使训练有素的缉毒犬闻到毒品的气味,故选项解释正确.
B、変瘪的乒乓球放入热水中能鼓起来,是因为温度升高,分子间的间隔变大,故选项解释错误.
C、原子总是在不断的运动的,铝制品中的铝原子是在不断的运动的,故选项解释错误.
D、将石块研磨成粉状,石块、石粉是宏观的物质,不能说明分子变小了,故选项解释错误.
故选:A.
点评 本题难度不大,掌握分子的基本性质(可以简记为:“两小运间,同同不不”)及利用分子的基本性质分析和解决问题的方法是解答此类题的关键.

练习册系列答案
相关题目
12.下列各组物质中,所含分子数相同的是( )
| A. | 224mL H2(标准状况)和0.5molN2 | B. | 5.6L N2(标准状况)和5.6g CO2 | ||
| C. | 11.2L H2O(标准状况)和0.5molBr2 | D. | 10g N2和10g CO |
19.下列说法正确的是( )
| A. | 溶液一定是无色透明的混合物 | |
| B. | 溶质质量分数是溶质质量与溶剂质量之比 | |
| C. | 溶液加水稀释前后,溶质的质量不变 | |
| D. | 均一、稳定的液体都是溶液 |
16.甲同学家新换了水龙头,从说明书上了解到该水龙头是铜质镀铬的.她想到在学过的金属活动性顺序中并没有金属铬,为比较铬与常见金属铁、铜的活动性强弱,她和同学们在应用所学知识进行分析的基础上,提出了以下猜想,并进行了实验探究.
【作出猜想】猜想1:Cr>Fe>Cu; 猜想2:Fe>Cu>Cr;
猜想3:你的猜想是Fe>Cr>Cu.
【查阅资料】①铬(Cr)是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜.②铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液.
【实验药品】铁片、铬片、铜片、稀硫酸、CuSO4溶液、CrSO4溶液、FeSO4溶液.(溶液均为新制)【甲同学实验】甲同学取大小相等的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的稀硫酸.
【乙同学实验】乙同学为验证甲同学的结论,又设计了以下实验.
【作出猜想】猜想1:Cr>Fe>Cu; 猜想2:Fe>Cu>Cr;
猜想3:你的猜想是Fe>Cr>Cu.
【查阅资料】①铬(Cr)是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜.②铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液.
【实验药品】铁片、铬片、铜片、稀硫酸、CuSO4溶液、CrSO4溶液、FeSO4溶液.(溶液均为新制)【甲同学实验】甲同学取大小相等的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的稀硫酸.
| 实验 | 实验操作 | 实验现象 | 结论与解释 |
| 试管1 | 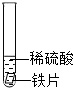 | 铁片表面产生气泡较慢, 溶液变为浅绿色 | (1)实验前用砂纸打磨金属片的目的是去除金属表面的污物和氧化物等. (2)甲同学得到的结论是猜想①正确 |
| 试管2 | 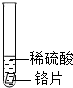 | 铬片表面产生气泡较快, 溶液变为蓝色 | |
| 试管3 | 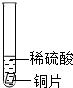 | 铜和稀硫酸不反应 |
| 实验 | 实验操作 | 实验现象 | 结论与解释 |
| 试管4 | 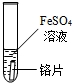 | 浅绿色的硫酸亚铁溶液变成蓝色,铬表面有红色物质生成 | (1)甲同学的结论正确 (2)请写出铬与硫酸铜反应的化学方程式Cr+CuSO4=CrSO4+Cu |
| 试管5 | 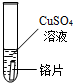 |
13.下列图象能正确反映对应变化关系的是( )
| A. | 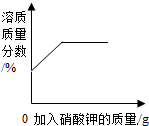 20℃时,向一定量的水中不断加入硝酸钾固体 | |
| B. | 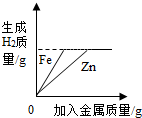 向等质量等质量分数的稀硫酸中分别加入足量等质量的锌和铁 | |
| C. | 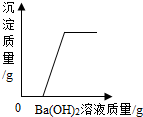 向盐酸和硫酸钠的混合溶液中逐滴加入氢氧化钡溶液 | |
| D. |  向盛有少量二氧化锰的烧杯中不断加入过氧化氢溶液 |
14.酸、碱、盐都是重要的化合物,请回答下列有关问题.
(1)碳酸钠溶液显碱性,请简述测定该溶液pH的操作方法用玻璃棒蘸取少量待测液滴在干燥的pH试纸上,与标准比色卡对比来确定pH.
(2)下列不属于复分解反应发生条件的是C(填字母).
A.有水生成
B.有气体生成
C.有单质生成
D.有沉淀生成
(3)某化学兴趣小组用一定量的碳酸钠溶液和石灰水反应制取氢氧化钠,并对反应后的溶液成分进行探究.
【提出问题】反应后的溶液中含有哪些溶质?
【做出猜想】甲:NaOH;乙:NaOH、Ca(OH)2;丙:NaOH、Na2CO3、Ca(OH)2;丁:NaOH、Na2CO3.
【交流表达】甲、乙、丙中不合理的猜想及其原因是丙,碳酸钠和氢氧化钙不能共存.
【实验探究】同学们进行了如下实验探究,请将表格内容填写完整.
(4)为测定某纯碱样品(含少量氯化钠杂质)中碳酸钠的含量,取12g样品放入烧杯中,加入100g稀盐酸,恰好完全反应.经测定,所得溶液质量为107.6g.请计算稀盐酸中溶质的质量分数.
(1)碳酸钠溶液显碱性,请简述测定该溶液pH的操作方法用玻璃棒蘸取少量待测液滴在干燥的pH试纸上,与标准比色卡对比来确定pH.
(2)下列不属于复分解反应发生条件的是C(填字母).
A.有水生成
B.有气体生成
C.有单质生成
D.有沉淀生成
(3)某化学兴趣小组用一定量的碳酸钠溶液和石灰水反应制取氢氧化钠,并对反应后的溶液成分进行探究.
【提出问题】反应后的溶液中含有哪些溶质?
【做出猜想】甲:NaOH;乙:NaOH、Ca(OH)2;丙:NaOH、Na2CO3、Ca(OH)2;丁:NaOH、Na2CO3.
【交流表达】甲、乙、丙中不合理的猜想及其原因是丙,碳酸钠和氢氧化钙不能共存.
【实验探究】同学们进行了如下实验探究,请将表格内容填写完整.
| 实验步骤 | 现象及化学反应方程式 | 结论 |
| 取少量反应后溶液于试管中,滴加碳酸钠溶液 | 产生白色沉淀,Ca(OH)2+Na2CO3=CaCO3↓+2NaOH | 猜想乙正确 |
 合金是重要的金属材料.
合金是重要的金属材料.