题目内容
19.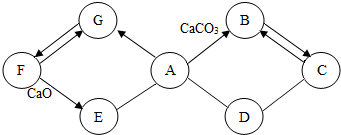 如图所示A~G是初中化学常见的物质.图中“→”表示转化关系,“-”表示相互能反应.已知A是人体胃液中含有的酸,G是最轻的气体,B和C含有相同的元素.
如图所示A~G是初中化学常见的物质.图中“→”表示转化关系,“-”表示相互能反应.已知A是人体胃液中含有的酸,G是最轻的气体,B和C含有相同的元素.(1)写出F的化学式H2O,E物质的一种用途改良酸性土壤等,C物质的一条化学性质具有可燃性、还原性.
(2)若D是赤铁矿的主要成分,写出C和D发生反应的化学方程式:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(3)A和E反应的化学方程式是Ca(OH)2+2HCl=CaCl2+2H2O.
分析 根据A~G是初中化学常见的物质,A是人体胃液中含有的酸,所以A是盐酸,G是最轻的气体,所以G是氢气,氢气和F可以相互转化,F会与氧化钙反应,所以F是水,水和氧化钙反应生成氢氧化钙,所以E是氢氧化钙,盐酸和碳酸钙反应生成氯化钙、水和二氧化碳,B和C含有相同的元素,可以相互转化,所以B是二氧化碳,C是一氧化碳,C和D之间的反应需要高温条件,所以D是氧化铁,一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳,然后将推出的各种物质代入转化关系中验证即可.
解答 解:(1)A~G是初中化学常见的物质,A是人体胃液中含有的酸,所以A是盐酸,G是最轻的气体,所以G是氢气,氢气和F可以相互转化,F会与氧化钙反应,所以F是水,水和氧化钙反应生成氢氧化钙,所以E是氢氧化钙,氢氧化钙可以用于改良酸性土壤等;盐酸和碳酸钙反应生成氯化钙、水和二氧化碳,B和C含有相同的元素,可以相互转化,所以B是二氧化碳,C是一氧化碳,C和D之间的反应需要高温条件,所以D是氧化铁,一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳,经过验证,推出的各种物质均满足题中的转化关系,推导正确,所以F是H2O,E是氢氧化钙,可以用来改良酸性土壤,一氧化碳具有可燃性、还原性;
(2)一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳,化学方程式为:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(3)A和E发生的反应是氢氧化钙和盐酸反应生成氯化钙和水,化学方程式为:Ca(OH)2+2HCl=CaCl2+2H2O.
故答案为:(1)H2O;改良酸性土壤等;具有可燃性、还原性;
(2)3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(3)Ca(OH)2+2HCl=CaCl2+2H2O.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

 据中青网报道,在山东东营利津县城附近,不少村民用6米长的塑料袋灌装天然气带回家,令不少路人为此举捏汗.路人称,这样带着天然气回家存在着较大的安全隐患.其中天然气的主要成分是( )
据中青网报道,在山东东营利津县城附近,不少村民用6米长的塑料袋灌装天然气带回家,令不少路人为此举捏汗.路人称,这样带着天然气回家存在着较大的安全隐患.其中天然气的主要成分是( )| A. | 氢气 | B. | 一氧化碳 | C. | 甲烷 | D. | 氧气 |
| A. | 酸能使紫色石蕊试液变红,通入CO2后的紫色石蕊试液变红,所以CO2是酸 | |
| B. | NaOH溶液能使无色酚酞试液变红色,Cu(OH) 2也能使无色酚酞试液变红色 | |
| C. | 碱溶液的pH都大于7,但pH大于7的溶液不一定是碱溶液 | |
| D. | 中和反应生成盐和水,则生成盐和水的反应一定是中和反应 |
| A. | 核外电子数 | B. | 核内质子数 | C. | 相对原子量 | D. | 最外层电子数 |
| A. | SO2和CO2 | B. | CO2和CO | C. | CO | D. | SO2和CO |
 如图是关于铜及其化合物的知识网络图.“→”表示一种物质转化为另一种物质.A、B、C分别是不同类别的铜的化合物,其中A物质为黑色粉末,B物质易溶于水.
如图是关于铜及其化合物的知识网络图.“→”表示一种物质转化为另一种物质.A、B、C分别是不同类别的铜的化合物,其中A物质为黑色粉末,B物质易溶于水.