题目内容
(12分)铁及其化合物在日常生活中随处可见。
(1)该同学用开水为爷爷泡茶时发现茶杯内有一不锈钢网,可以防止将茶叶直接喝进嘴里。使用该网类似于进行化学实验中的 操作。
(2)该同学奶奶用开水泡制一种含铁粉的麦片,食用后在胃酸(盐酸)作用下将铁粉转化为人体可吸收的铁元素,反应的化学方程式为 ,该反应属于 反应(填基本反应类型).
(3)铝锅比铁锅更耐腐蚀,其原因是 。
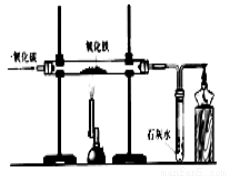
(4)工业上常采用一氧化碳与赤铁矿(主要成分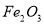 )为原料炼铁,写出该反应的化学方程式: ;实验室可用下图所示的装置进行该实验.实验过程中,要先通一氧化碳,后加热,原因是
)为原料炼铁,写出该反应的化学方程式: ;实验室可用下图所示的装置进行该实验.实验过程中,要先通一氧化碳,后加热,原因是
(5)某钢铁厂每天需消耗5000t含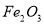 76%的赤铁矿石,该厂理论上可日产含Fe 98%的生铁 t.
76%的赤铁矿石,该厂理论上可日产含Fe 98%的生铁 t.
(计算结果精确至0.1)
(1)过滤;(2)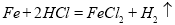 ↑; 置换;(3)铝锅表面有一层致密的氧化膜;(4)
↑; 置换;(3)铝锅表面有一层致密的氧化膜;(4)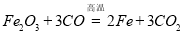 ;将玻璃管中的空气排尽,避免发生爆炸;(5)2714.3
;将玻璃管中的空气排尽,避免发生爆炸;(5)2714.3
【解析】
试题分析:(1)过滤可以除去液体中的不溶性固体物质;(2)胃酸的成分是盐酸,铁和盐酸反应生成氯化亚铁和氢气,该反应是置换反应;(3)铝和氧气反应生成的氧化铝是一层结构致密的氧化物,可以隔绝空气和水分从而对金属有保护作用,而铁锈是一种疏松多孔的物质,铁生锈后会加快铁的腐蚀;(4)一氧化碳和氧化铁在高温下生成铁和二氧化碳;一氧化碳是一种可燃性的气体,和空气混合加热易发生爆炸,故用一氧化碳来还原氧化铁时,先通一氧化碳将装置内的空气排出,防止加热发生爆炸;
(5)5000t含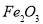 76%的赤铁矿石中氧化铁的质量=5000t×76%=3800t;设生成铁的质量为x
76%的赤铁矿石中氧化铁的质量=5000t×76%=3800t;设生成铁的质量为x
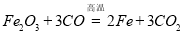
160 112
3800t x
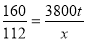
x=2660t
生铁的质量=2660t÷98%≈2714t
考点:过滤;金属的化学性质;反应类型;铁的冶炼;根据化学方程式的计算;

(8分)目前市场上的补钙药剂很多,下图是某品牌补钙药品的部分说明书.

为测定其含量是否达标,某兴趣小组的同学取10片钙片研碎后放于烧杯中,将100g稀盐酸分五次加入到烧杯中,并不断搅拌,称量,将得到的有关数据记录如下(钙片中其它成分不与稀盐酸反应):
加入稀盐酸的质量/g | 0 | 20 | 40 | 60 | 80 | 100 |
烧杯中剩余物质质量/g | 10 | 29.12 | 48.24 | 67.36 | 86.48 | 106.48 |
请你根据题给信息和表中数据,回答下列问题:
(1)实验过程中将钙片研碎的目的是: .
(2)完全反应后,产生二氧化碳的质量为 g.
(3)试通过计算说明,该品牌钙片含量是否达标.(写出计算过程)
(4)如果按用量服用,服用者每天通过该补钙剂摄入钙元素的质量为 g.

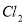 消毒会促使一些致癌物质的生成,为了消除隐患,提高生活质量,现在已经采用高效安全的
消毒会促使一些致癌物质的生成,为了消除隐患,提高生活质量,现在已经采用高效安全的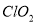 消毒杀菌.
消毒杀菌.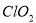 是由分子构成的物质,下列对
是由分子构成的物质,下列对