题目内容
用铁屑、铜粉、高锰酸钾、稀盐酸四种物质为原料,采取两种不同的方法制取氯化亚铁,请写出各步化学方程式.
考点:书写化学方程式、文字表达式、电离方程式
专题:化学用语和质量守恒定律
分析:铁的金属活动性比氢强,能与稀盐酸反应生成氯化亚铁和氢气;铜在加热条件下与氧气反应生成氧化铜,氧化铜与稀盐酸反应生成氯化铜和水,铁能与氯化铜反应生成氯化亚铁和铜;据此进行分析解答.
解答:解:方案一:铁的金属活动性比氢强,能与稀盐酸反应生成氯化亚铁和氢气,反应的化学方程式为:Fe+2HCl═FeCl2+H2↑.
方案二:铜在加热条件下与空气中的氧气反应生成氧化铜,反应的化学方程式是2Cu+O2
2CuO.
氧化铜与稀盐酸反应生成氯化铜和水,反应的化学方程式是CuO+2HCl=CuCl2+H2O.
铁能与氯化铜反应生成氯化亚铁和铜,反应的化学方程式是Fe+CuCl2=FeCl2+Cu.
故答案为:方案一:Fe+2HCl═FeCl2+H2↑;方案二:2Cu+O2
2CuO;CuO+2HCl=CuCl2+H2O;Fe+CuCl2=FeCl2+Cu.
方案二:铜在加热条件下与空气中的氧气反应生成氧化铜,反应的化学方程式是2Cu+O2
| ||
氧化铜与稀盐酸反应生成氯化铜和水,反应的化学方程式是CuO+2HCl=CuCl2+H2O.
铁能与氯化铜反应生成氯化亚铁和铜,反应的化学方程式是Fe+CuCl2=FeCl2+Cu.
故答案为:方案一:Fe+2HCl═FeCl2+H2↑;方案二:2Cu+O2
| ||
点评:本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

练习册系列答案
相关题目
 人体缺少钙元素会影响健康,因此每日需摄入足够的钙.市场上某补钙制剂的说明书如下图所示,请仔细阅读,并进行计算.
人体缺少钙元素会影响健康,因此每日需摄入足够的钙.市场上某补钙制剂的说明书如下图所示,请仔细阅读,并进行计算. 乙炔俗称电石气,是因为电石(CaC2)遇水可产生乙炔(C2H2)气体,反应的化学方程式为CaC2+2H2O=Ca(OH)2+C2H2↑某桶电石标签的部分内容如图所示.计算:
乙炔俗称电石气,是因为电石(CaC2)遇水可产生乙炔(C2H2)气体,反应的化学方程式为CaC2+2H2O=Ca(OH)2+C2H2↑某桶电石标签的部分内容如图所示.计算: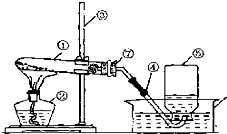 如图是实验室里用加热高锰酸钾的方法制取氧气的实验装置图.
如图是实验室里用加热高锰酸钾的方法制取氧气的实验装置图.
 通常用如图所示的方法进行气密性检查,如果装置不漏气,可看到
通常用如图所示的方法进行气密性检查,如果装置不漏气,可看到 某化肥包装袋上的部分说明如图所示.
某化肥包装袋上的部分说明如图所示.