题目内容
16.图1是配制溶质质量分数为10%的NaCl溶液的实验操作示意图: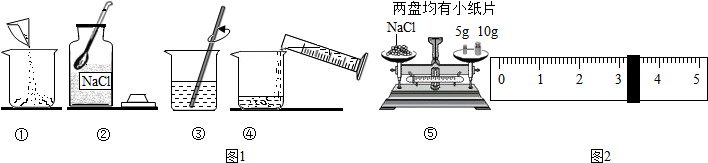
(1)用图1的序号表示配制溶液的正确操作顺序为②⑤①④③.
(2)操作③用玻璃棒搅拌的目的是加速氯化钠溶解.
(3)称量NaCl时,天平平衡后的状态如图所示,游码标尺示数见右图,则需要量取水的体积是163.8(水的密度为1g/mL).
分析 (1)图①操作为把称取的氯化钠倒入烧杯,图②的操作为用药匙取氯化钠,图③操作为用玻璃棒搅拌溶解氯化钠,图④操作为把量取的水倒入盛有氯化钠的烧杯中,图⑤操作为称取氯化钠;根据利用固体溶质氯化钠配制溶液的步骤,对操作进行排序;
(2)溶解时玻璃棒的作用是加速固体溶解;
(3)砝码与游码的质量和为所称氯化钠的质量,游码读数时应以游码左侧数值为准;利用所称取溶质氯化钠的质量和所要配制溶液的溶质质质量分数,根据溶质质量分数计算公式,求出所要配制溶液的质量,溶液质量与溶质质量差即为溶剂水的质量,进而确定水的体积.
解答 解:(1)根据用固体溶质氯化钠配制溶液的步骤:计算-称量-溶解,先取氯化钠进行称取,倒入烧杯;然后量取水,倒入盛氯化钠的烧杯中;最后进行溶解;
故答案为:②⑤①④③;
(2)溶解时玻璃棒的作用是加速固体溶解;
故答案为:加速氯化钠溶解;
(3)砝码的质量为10g+5g=15g,游码的质量为3.2g,所称取氯化钠的质量=15g+3.2g=18.2g;
所配制溶液的质量=18.2g/10%=182g,则需要水的质量=182g-18.2g=163.8g,由于水的密度是1g/mL,故需要水的体积为:163.8mL;
故答案为:163.8
点评 本题对使用氯化钠配制溶液实验进行了考查,其中涉及溶液配制的步骤、溶液组成的计算、天平的使用,难度不大

练习册系列答案
 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案
相关题目
4.下列属于纯净物的是( )
| A. | 生铁 | B. | 矿泉水 | C. | 硬水 | D. | 蒸馏水 |
1.下列原子中的粒子,带负电荷的是( )
| A. | 电子 | B. | 中子 | C. | 质子 | D. | 原子核 |
8.阅读下面科普短文.
亚硝酸盐广泛存在于自然环境和我们的生活中,就像空气一样平凡.在粮食、豆类、蔬菜、肉类、蛋类等食物中,都可以检测出一定量的亚硝酸盐.蔬菜中一般都含有硝酸盐,含量高的是茎叶类蔬菜、其次是根茎类蔬菜、然后是瓜类蔬菜,它们在煮熟后如果久置,硝酸盐就会被分解为亚硝酸盐.
大剂量的亚硝酸盐能够将人体内血红素中的铁元素由+2价氧化为+3价,从而使其失去携氧能力,引起全身组织缺氧,即产生亚硝酸盐中毒.当体内+3价铁血红蛋白达到20%~40%就会出现缺氧症状,达到70%以上可导致死亡.
亚硝酸盐控制在安全范围内使用,是不会对身体造成危害的,而且它对预防致命的肉毒梭菌中毒具有不可替代的作用.我国和许多国家都批准把亚硝酸盐作为食品添加剂以防止食品腐败、改进肉类颜色.亚硝酸盐与肌肉中的乳酸作用会产生亚硝胺,亚硝胺不稳定易分解产生一氧化氮,一氧化氮与肌红蛋白结合产生红色的亚硝基肌红蛋白,使肉制品产生稳定的红色.
为了测定煮熟后的蔬菜中亚硝酸盐含量,研究人员选用白菜进行了测定.实验1温度为20℃,实验2温度为13℃,实验中分别取放置2、4、6、8、10、12、24小时的熟白菜汁3滴,滴入1滴稀硫酸,再滴入2滴0.03%高锰酸钾溶液,若溶液的紫红色褪去,表示含有亚硝酸盐.实验记录见下表:
依据文章内容,回答下列问题.
(1)高锰酸钾溶液中的溶质是高锰酸钾.
(2)亚硝酸盐使人体中毒的原因亚硝酸盐能将人体内血红素中铁元素由+2价氧化为+3价,从而使其失去携氧能力,引起全身组织缺氧.
(3)下列有关亚硝酸盐的说法正确的是AC(填字母序号).
A.煮熟蔬菜中的硝酸盐会被逐渐分解为亚硝酸盐
B.温度越低,熟蔬菜中亚硝酸盐产生的速率越快
C.亚硝酸盐与肌肉中的乳酸作用产生亚硝胺发生的是化学变化
(4)为了减少蔬菜中硝酸盐的含量,在种植过程中应该适当减少氮肥的施用.
(5)根据实验现象,你对一次吃不完的熟蔬菜的建议是低温下贮存;②尽早食用.
亚硝酸盐广泛存在于自然环境和我们的生活中,就像空气一样平凡.在粮食、豆类、蔬菜、肉类、蛋类等食物中,都可以检测出一定量的亚硝酸盐.蔬菜中一般都含有硝酸盐,含量高的是茎叶类蔬菜、其次是根茎类蔬菜、然后是瓜类蔬菜,它们在煮熟后如果久置,硝酸盐就会被分解为亚硝酸盐.
大剂量的亚硝酸盐能够将人体内血红素中的铁元素由+2价氧化为+3价,从而使其失去携氧能力,引起全身组织缺氧,即产生亚硝酸盐中毒.当体内+3价铁血红蛋白达到20%~40%就会出现缺氧症状,达到70%以上可导致死亡.
亚硝酸盐控制在安全范围内使用,是不会对身体造成危害的,而且它对预防致命的肉毒梭菌中毒具有不可替代的作用.我国和许多国家都批准把亚硝酸盐作为食品添加剂以防止食品腐败、改进肉类颜色.亚硝酸盐与肌肉中的乳酸作用会产生亚硝胺,亚硝胺不稳定易分解产生一氧化氮,一氧化氮与肌红蛋白结合产生红色的亚硝基肌红蛋白,使肉制品产生稳定的红色.
为了测定煮熟后的蔬菜中亚硝酸盐含量,研究人员选用白菜进行了测定.实验1温度为20℃,实验2温度为13℃,实验中分别取放置2、4、6、8、10、12、24小时的熟白菜汁3滴,滴入1滴稀硫酸,再滴入2滴0.03%高锰酸钾溶液,若溶液的紫红色褪去,表示含有亚硝酸盐.实验记录见下表:
| 时间/h | 2 | 4 | 6 | 8 | 10 | 12 | 24 |
| 实验1 | 不褪色 | 不褪色 | 不褪色 | 由稍褪色到褪色且速度逐渐加快 | |||
| 实验2 | 不褪色 | 不褪色 | 不褪色 | 不褪色 | 不褪色 | 褪色且速度加快 | |
(1)高锰酸钾溶液中的溶质是高锰酸钾.
(2)亚硝酸盐使人体中毒的原因亚硝酸盐能将人体内血红素中铁元素由+2价氧化为+3价,从而使其失去携氧能力,引起全身组织缺氧.
(3)下列有关亚硝酸盐的说法正确的是AC(填字母序号).
A.煮熟蔬菜中的硝酸盐会被逐渐分解为亚硝酸盐
B.温度越低,熟蔬菜中亚硝酸盐产生的速率越快
C.亚硝酸盐与肌肉中的乳酸作用产生亚硝胺发生的是化学变化
(4)为了减少蔬菜中硝酸盐的含量,在种植过程中应该适当减少氮肥的施用.
(5)根据实验现象,你对一次吃不完的熟蔬菜的建议是低温下贮存;②尽早食用.
5.关于实验室用过氧化氢、氯酸钾、高锰酸钾制取氧气的反应,下列说法正确的是( )
| A. | 都需要加热 | B. | 都需要催化剂 | ||
| C. | 都有元素化合价的升降 | D. | 都有氧化物生成 |
17.归纳、总结是重要的学习方法.下列说法中正确的是( )
| A. | 酸中一定含氧元素 | B. | 含氧的化合物一定是氧化物 | ||
| C. | 盐中一定含金属元素 | D. | 碱中一定含氢元素和氧元素 |