题目内容
6.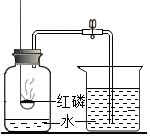 如图装置测定空气里氧气的含量.若一切操作规范,则实验完毕后烧杯中的水进入集气瓶,瓶中进入的水约占集气瓶容积的$\frac{1}{5}$.反应的化学表达式为4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
如图装置测定空气里氧气的含量.若一切操作规范,则实验完毕后烧杯中的水进入集气瓶,瓶中进入的水约占集气瓶容积的$\frac{1}{5}$.反应的化学表达式为4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
分析 本题是测定空气中氧气的含量,我们常用燃烧红磷或白磷的方法,因为磷燃烧生成白色固体五氧化二磷,几乎不占空间,使得内外产生气压差,从而得到正确的结论.因此在选择可燃物时,必须考虑到:燃烧的条件;生成物的状态;不与空气中其他物质发生反应.保证本实验成功的关键是:①装置气密性好;②红磷要足量;③要冷却至室温再读数.
解答 解:红磷燃烧消耗氧气,集气瓶内压强减小,外界气压将水沿导管压入集气瓶,倒流入水的体积等于减少的氧气的体积,大约占集气瓶体积的五分之一;磷与氧气在点燃条件下反应生成五氧化二磷,反应的化学表达式为:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
答案:$\frac{1}{5}$;4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
点评 本题主要考查用红磷测定空气组成的实验原理、操作、现象、结论和注意事项,难度稍大.

练习册系列答案
相关题目
16.在平衡的杠杆两端各系-个等量的铁球,分别浸没在稀硫酸和硫酸铜溶液中将看到( )
| A. | 杠杆最终向稀硫酸一边下沉 | B. | 杠杆会上下摇摆,但最终保持平衡 | ||
| C. | 杠杆最终向硫酸铜溶液一边下沉 | D. | 无法确定 |
14.许多化学物质是一柄双刃剑,对二氧化碳的利弊评价不妥的是( )
| A. | 大气中CO2过多会造成环境污染 | |
| B. | “碳酸水”浇灌植物对植物光合作用、碱性土壤改良有利 | |
| C. | 利用干冰可进行人工降雨 | |
| D. | 大气层中CO2越多,抵御紫外线的作用越强 |
11.下列过程中主要发生物理变化的是( )
| A. |  氯化钠溶液导电 | B. |  碱与指示剂作用 | C. |  自制白糖晶体 | D. |  自制的叶脉书签 |
16.下列符号中,只有微观意义而没有宏观意义的是( )
| A. | Fe | B. | O2 | C. | O2- | D. | H2O |