题目内容
15.硫酸铜溶液对过氧化氢的分解有催化作用.取一定量8.5%的过氧化氢溶液倒入小烧杯中,向其中加入15%的硫酸铜溶液6.6g,使过氧化氢完全分解,反应后称量溶液的质量减少了1.6g.(不考了气体在水中的溶解)计算:
(1)共产生氧气1.6g.
(2)加入过氧化氢溶液的质量(写出计算过程).
分析 过氧化氢在硫酸铜溶液的催化作用下生成水和氧气,由质量守恒定律,混合物减少的质量即为生成氧气的质量,由反应的化学方程式,列式计算出参加反应的过氧化氢的质量即可.
解答 解:(1)由质量守恒定律,生成氧气的质量为1.6g.
(2)设参加反应的过氧化氢的质量为x
2H2O2$\frac{\underline{\;CuSO_{4}\;}}{\;}$2H2O+O2↑
68 32
x 1.6g
$\frac{68}{32}=\frac{x}{1.6g}$ x=3.4g
加入过氧化氢溶液的质量为3.4g÷8.5%=40g.
答:(1)1.6;(2)加入过氧化氢溶液的质量为40g.
点评 本题难度不大,掌握根据化学方程式的计算即可正确解答本题,根据质量守恒定律计算出氧气的质量是正确解答本题的前提和关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.下列物质的用途,主要利用了物质化学性质的是( )
| A. | 水作溶剂 | B. | 熟石灰用于改良酸性土壤 | ||
| C. | 氦气用于填充气球 | D. | 铜用于制导线 |
6.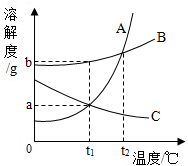 如图为A、B、C三种固体物质的溶解度曲线.下列有关说法错误的是( )
如图为A、B、C三种固体物质的溶解度曲线.下列有关说法错误的是( )
 如图为A、B、C三种固体物质的溶解度曲线.下列有关说法错误的是( )
如图为A、B、C三种固体物质的溶解度曲线.下列有关说法错误的是( )| A. | t1℃三种物质中B物质的溶解度大 | |
| B. | t2℃三种物质的饱和溶液中,溶质的质量分数最大的是A | |
| C. | t2℃时可用降低温度的方法使C的不饱和溶液变为饱和溶液 | |
| D. | t1℃时,A、C两种物质的溶解度相等 |
3.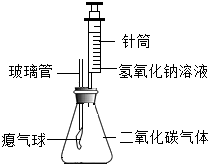 用如图装置探究氢氧化钠溶液与二氧化碳气体的反应.(已知:NaHCO3+NaOH═Na2CO3+H2O)
用如图装置探究氢氧化钠溶液与二氧化碳气体的反应.(已知:NaHCO3+NaOH═Na2CO3+H2O)
(1)将针筒中的氢氧化钠溶液压入锥形瓶中,振荡,观察到的现象是瘪气球胀大.
(2)部分同学对实验后锥形瓶中溶液的溶质是什么提出疑问?同学们有如下猜想:
猜想一:碳酸钠
猜想二:氢氧化钠和碳酸钠
猜想三:碳酸钠和碳酸氢钠
猜想四:碳酸氢钠
【实验设计】为了验证猜想二是否正确,甲同学设计如下实验,请你帮助该同学将实验设计补充完整.
(3)经同学讨论,认为上述实验设计不合理,理由是NaOH+HCl=NaCl+H2O(用化学方程式表示).
(4)请设计合理的实验方案验证猜想二,简要叙述实验步骤:取少量该溶液于试管中,加入过量的氯化钙溶液,静置,取上层清液于另一只试管中,加入几滴酚酞试液.
(5)【反思拓展】在分析化学反应后所得物质的成分时,除了考虑生成物外还需考虑反应物量的关系.
 用如图装置探究氢氧化钠溶液与二氧化碳气体的反应.(已知:NaHCO3+NaOH═Na2CO3+H2O)
用如图装置探究氢氧化钠溶液与二氧化碳气体的反应.(已知:NaHCO3+NaOH═Na2CO3+H2O)(1)将针筒中的氢氧化钠溶液压入锥形瓶中,振荡,观察到的现象是瘪气球胀大.
(2)部分同学对实验后锥形瓶中溶液的溶质是什么提出疑问?同学们有如下猜想:
猜想一:碳酸钠
猜想二:氢氧化钠和碳酸钠
猜想三:碳酸钠和碳酸氢钠
猜想四:碳酸氢钠
【实验设计】为了验证猜想二是否正确,甲同学设计如下实验,请你帮助该同学将实验设计补充完整.
| 实验内容 | 预计现象 | 获得结论 |
| ①取少量锥形瓶中的溶液于试管中,加入过量稀盐酸 | 试管中有气泡产生 | 证明溶液中含有碳酸钠 |
| ②继续往试管中滴加无色酚酞溶液 | 无明显现象 | 证明溶液中不含氢氧化钠 |
(4)请设计合理的实验方案验证猜想二,简要叙述实验步骤:取少量该溶液于试管中,加入过量的氯化钙溶液,静置,取上层清液于另一只试管中,加入几滴酚酞试液.
(5)【反思拓展】在分析化学反应后所得物质的成分时,除了考虑生成物外还需考虑反应物量的关系.
 目前哈尔滨市地铁三号线一期工程铺轨工作己完成60%,预计8月份将实现“轨通”.请回答问题:
目前哈尔滨市地铁三号线一期工程铺轨工作己完成60%,预计8月份将实现“轨通”.请回答问题: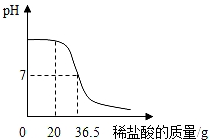 某化学兴趣小组在实验室配制一定溶质质量分数的稀盐酸,并用其测定某氢氧化钠溶液的溶质的质量分数.
某化学兴趣小组在实验室配制一定溶质质量分数的稀盐酸,并用其测定某氢氧化钠溶液的溶质的质量分数.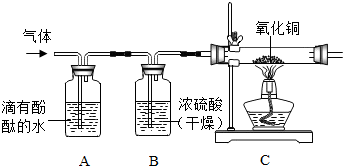
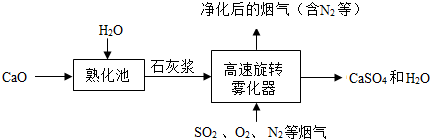
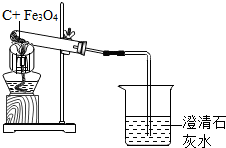 资料显示:碳还原四氧化三铁制得铁的温度在700℃~800℃.某校化学兴趣小组在探究用碳冶炼铁的原理的实验时,取一定质量的碳粉和四氧化三铁粉的混合物,在700℃--800℃的高温条件下使其充分
资料显示:碳还原四氧化三铁制得铁的温度在700℃~800℃.某校化学兴趣小组在探究用碳冶炼铁的原理的实验时,取一定质量的碳粉和四氧化三铁粉的混合物,在700℃--800℃的高温条件下使其充分