题目内容
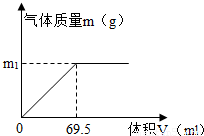
某固体混合物由碳酸钙和氯化钙均匀混合而成,取31.4g该混合物,向其中逐滴加入10%的盐酸溶液(密度为1.05g/cm3),生成气体的质量m与所用稀盐酸的体积v有如图所示关系(氯化钙不与盐酸反应) 求:(1)原混合物中碳酸钙的质量分数
(2)m1数值
(3)混合物与稀盐酸恰好完全反应时所得溶液中溶质的质量分数(计算过程中精确到0.1)
【答案】分析:根据反应时的盐酸的体积以及盐酸的密度可以计算出反应的氯化氢的质量,则利用方程式可以计算出反应中碳酸钙和二氧化碳的质量,据此解答即可;
解答:解:由图示可知恰好反应的氯化氢质量为69.5mL×1.05g/mL×10%=7.3g;
设原混合物中碳酸钙的质量为x生成二氧化碳的质量是y氯化钙的质量是z
CaCO3 +2HCl=CaCl2 +H2O+CO2↑
100 73 111 44
x 7.2975g z y
 ;
;
x=10g z=11.1g y=4.4g
(1)原混合物中碳酸钙的质量分数为= ×100%≈31.8%;
×100%≈31.8%;
(2)m1数值为4.4;
(3)原混合物中氯化钙的质量为31.4g-10g=21.4g,所得溶液的质量为31.4g+73g-4.4g=100g,则混合物与稀盐酸恰好完全反应时所得溶液中溶质的质量分数为 ×100%=32.4%;
×100%=32.4%;
答:(1)(1)原混合物中碳酸钙的质量分数31.8%;
(2)m1数值为4.4;
(3)混合物与稀盐酸恰好完全反应时所得溶液中溶质的质量分数32.4%;
点评:本题难度较大,主要考查了以化学方程式计算为基础,同时融入溶液等方面的计算题,这样的题目一直是中考的热点,主要培养学生的综合分析能力和计算能力;
解答:解:由图示可知恰好反应的氯化氢质量为69.5mL×1.05g/mL×10%=7.3g;
设原混合物中碳酸钙的质量为x生成二氧化碳的质量是y氯化钙的质量是z
CaCO3 +2HCl=CaCl2 +H2O+CO2↑
100 73 111 44
x 7.2975g z y
 ;
;x=10g z=11.1g y=4.4g
(1)原混合物中碳酸钙的质量分数为=
 ×100%≈31.8%;
×100%≈31.8%;(2)m1数值为4.4;
(3)原混合物中氯化钙的质量为31.4g-10g=21.4g,所得溶液的质量为31.4g+73g-4.4g=100g,则混合物与稀盐酸恰好完全反应时所得溶液中溶质的质量分数为
 ×100%=32.4%;
×100%=32.4%;答:(1)(1)原混合物中碳酸钙的质量分数31.8%;
(2)m1数值为4.4;
(3)混合物与稀盐酸恰好完全反应时所得溶液中溶质的质量分数32.4%;
点评:本题难度较大,主要考查了以化学方程式计算为基础,同时融入溶液等方面的计算题,这样的题目一直是中考的热点,主要培养学生的综合分析能力和计算能力;

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
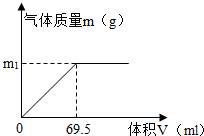 某固体混合物由碳酸钙和氯化钙均匀混合而成,取31.4g该混合物,向其中逐滴加入10%的盐酸溶液(密度为1.05g/cm3),生成气体的质量m与所用稀盐酸的体积v有如图所示关系(氯化钙不与盐酸反应) 求:
某固体混合物由碳酸钙和氯化钙均匀混合而成,取31.4g该混合物,向其中逐滴加入10%的盐酸溶液(密度为1.05g/cm3),生成气体的质量m与所用稀盐酸的体积v有如图所示关系(氯化钙不与盐酸反应) 求: 现有一瓶未开启的浓硫酸,试剂瓶标签上的部分内容如图所示.请根据有关信息回答并计算:
现有一瓶未开启的浓硫酸,试剂瓶标签上的部分内容如图所示.请根据有关信息回答并计算: