题目内容
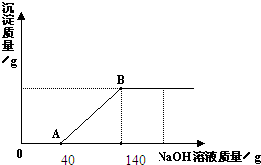 现有一瓶硫酸铜和稀硫酸的混合溶液,为测定溶液中硫酸铜的溶质质量分数,小强同学取用80g样品,并缓缓向样品中滴加10%的氢氧化钠溶液至过量.测得所加氢氧化钠溶液质量与生成的沉淀的质量关系如图所示:
现有一瓶硫酸铜和稀硫酸的混合溶液,为测定溶液中硫酸铜的溶质质量分数,小强同学取用80g样品,并缓缓向样品中滴加10%的氢氧化钠溶液至过量.测得所加氢氧化钠溶液质量与生成的沉淀的质量关系如图所示:(1)反应结束时,共消耗氢氧化钠溶液的质量为
(2)请列示算原混合溶液中所含硫酸铜的溶质质量分数.
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:(1)在有稀硫酸存在的情况下氢氧化铜不能以沉淀的形式析出,所以可以判断与稀硫酸反应的氢氧化钠的质量为40g,可以据此完成该题的解答;
(2)根据题意可以知道与硫酸铜反应的氢氧化钠溶液的质量为140g-40g=100g,可以据此结合氢氧化钠溶液的质量分数可以计算出硫酸铜的质量,进而计算出硫酸铜溶液中溶质的质量分数.
(2)根据题意可以知道与硫酸铜反应的氢氧化钠溶液的质量为140g-40g=100g,可以据此结合氢氧化钠溶液的质量分数可以计算出硫酸铜的质量,进而计算出硫酸铜溶液中溶质的质量分数.
解答:解:(1)由图中的信息可以知道加入的氢氧化钠溶液的质量为140g时沉淀的质量不再增加,所以可以判断共消耗的氢氧化钠溶液的质量为140g,在有稀硫酸存在的情况下氢氧化铜不能以沉淀的形式析出,所以可以判断与稀硫酸反应的氢氧化钠溶液的质量为40g;
(2)与硫酸铜反应的氢氧化钠的质量为:(140g-40g)×10%=10g
设硫酸铜的质量为x
2NaOH+CuSO4═Na2SO4+Cu(OH)2↓
80 160
10g x
=
解得:x=20g
原混合溶液中所含硫酸铜的溶质质量分数为:
×100%=25%
答:原混合溶液中所含硫酸铜的溶质质量分数为25%
故答案为:(1)140;40;
(2)25%.
(2)与硫酸铜反应的氢氧化钠的质量为:(140g-40g)×10%=10g
设硫酸铜的质量为x
2NaOH+CuSO4═Na2SO4+Cu(OH)2↓
80 160
10g x
| 80 |
| 10g |
| 160 |
| x |
解得:x=20g
原混合溶液中所含硫酸铜的溶质质量分数为:
| 20g |
| 80g |
答:原混合溶液中所含硫酸铜的溶质质量分数为25%
故答案为:(1)140;40;
(2)25%.
点评:数形结合类问题,在分析时反应的关系图的分析为正确判断反应进行的依据和基础.弄清折点的含义,是解决此题的关键之所在.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
在20℃时,某气态碳氢化合物与氧气混合后装入密闭容器中,经充分反应后,又恢复到20℃,此时容器内气体分子是反应前的一半.再经足量的氢氧化钠溶液吸收后,容器内几乎成真空.此碳氢化合物不可能是( )
| A、CH4 |
| B、C2H6 |
| C、C3H8 |
| D、C2H4 |
2013年12月2日“嫦娥三号”成功发射,它携“玉兔”号月球车首次实现月球软着陆和月面巡视勘察.下图表示发生火箭子三级发动机内氢气和氧气燃烧生产水的微观过程,下列说法错误的是( )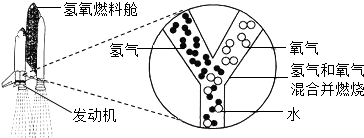

| A、氢气、氧气和水都是由分子构成的 |
| B、燃烧过程中,分子种类发生了改变 |
| C、燃烧过程中,原子的种类也发生了变化 |
| D、氢气和氧气燃烧生成水属于化合反应 |
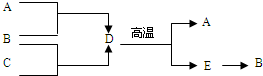 ABCDE五种物质均为初中化学中的常见物质,它们相互间有着如图所示的转化关系.已知A是光合作用的原料之一,B是改良酸性土壤常用的碱试回答下列问题:
ABCDE五种物质均为初中化学中的常见物质,它们相互间有着如图所示的转化关系.已知A是光合作用的原料之一,B是改良酸性土壤常用的碱试回答下列问题: 某同学欲探究市售“双钙防蛀”牙膏、“皓清”牙膏和牙粉的主要成分.
某同学欲探究市售“双钙防蛀”牙膏、“皓清”牙膏和牙粉的主要成分.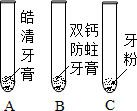
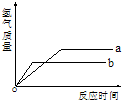 等质量的两种金属a、b分别与足量的稀硫酸反应,都生成+2价的化合物和氢气,其反应情况如图所示:
等质量的两种金属a、b分别与足量的稀硫酸反应,都生成+2价的化合物和氢气,其反应情况如图所示: