题目内容
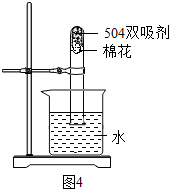
铁缓慢氧化生成Fe2O3,发生反应的化学方程式为4Fe+3O2=2Fe2O3,计算生成80g Fe2O3需要铁的质量(写出计算过程).
设需要铁的质量为x
4Fe+3O2═2Fe2O3
4×56 2×160
x 80g
=
x=56g
答:需要铁的质量为56g.
4Fe+3O2═2Fe2O3
4×56 2×160
x 80g
| 4×56 |
| x |
| 2×160 |
| 80g |
x=56g
答:需要铁的质量为56g.

练习册系列答案
 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案
相关题目