题目内容
1.菱铁矿的主要成分是FeCO3,下列说法正确的是( )| A. | FeCO3由五种元素组成 | |
| B. | FeCO3中Fe、C、O元素的质量比是1:l:3 | |
| C. | FeCO3的相对分子质量是84 | |
| D. | FeCO3中Fe元素的质量分数是48.3% |
分析 A、根据FeCO3化学式的含义进行分析判断.
B、根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析判断.
C、根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析判断.
D、根据化合物中元素的质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%,进行分析判断.
解答 解:A、FeCO3由铁、碳、氧三种元素组成,故选项说法错误.
B、FeCO3中Fe、C、O元素的质量比是(56×1):(12×1):(16×3)≠1:l:3,故选项说法错误.
C、FeCO3的相对分子质量是56+12+16×3=116,故选项说法错误.
D、FeCO3中Fe元素的质量分数是$\frac{56}{116}$×100%≈48.3%,故选项说法正确.
故选:D.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
12.下列探究活动没有采用控制变量法的是( )
| A. | 探究水的组成 | B. | 探究影响电阻大小的因素 | ||
| C. | 探究铁制品锈蚀的条件 | D. | 探究影响压力作用效果的因素 |
9.钛的熔点高,密度小,抗腐蚀性能好,在航天工业和化学工业中用途广泛,已知钛原子的核电荷数为22,中子数为26,则该原子的质子数和相对原子质量分别是( )
| A. | 48,26 | B. | 22,48 | C. | 26,48 | D. | 4,22 |
16.下列物质的用途主要由其化学性质决定的是( )
| A. | 用碳酸氢钠治疗胃酸过多 | B. | 用金刚石做玻璃刀的刀头 | ||
| C. | 用石墨做铅笔芯写字 | D. | 用钨做电灯泡里的灯丝 |
13.下列各组物质中的杂质除去方案合理的是( )
| 选项 | 杂质 | 除杂质所用试剂或方法 |
| A.H2 | HCl气体 | 先通过NaOH溶液,再通过浓硫酸 |
| B.NaOH | Ba(OH)2溶液 | 先加入CuSO4溶液、过滤 |
| C.CO | CO2气体 | 通过灼热的CuO |
| D.CuCl2 | Cu(OH)2 | 加入H2SO4 |
| A. | A | B. | B | C. | C | D. | D |
10.被称为“生命之源”的水(H2O)和被称为“绿色氧化剂”的双氧水(H2O2),都是由氢、氧两种元素组成的化合物,通常情况下均为无色液体.在化学实验开放日,实验小组的同学用下面的方法鉴别水和双氧水两瓶无色液体,请填写有关内容:
(1)B试管中发生反应的文字表达式:过氧化氢$\stackrel{二氧化锰}{→}$水+氧气
(2)如何验证B试管中产生的气体(写出操作步骤、实验现象和结论)?
操作步骤用带火星木条放在试管口
实验现象木条复燃
结论证明产生的气体是氧气.
| 实验步骤 | 实验现象 | 实验结论 |
| ①将等体积的两种无色液体分别加入A、B两个试管中. ②分别向A、B两试管中同时加入等质量(少量)的二氧化锰,观察现象. 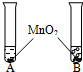 | A试管中无明显现象 B试管中有气泡产生 | A试管中的无色液体是: H2O; B试管中的无色液体是: H2O2; |
(2)如何验证B试管中产生的气体(写出操作步骤、实验现象和结论)?
操作步骤用带火星木条放在试管口
实验现象木条复燃
结论证明产生的气体是氧气.

