题目内容
16.40℃时,将等质量的甲、乙固体分别放入各盛有100g水的两个烧杯中,充分搅拌后并降温至20℃,现象如图1所示,有关甲和乙的溶解度曲线如图2所示.
(1)图1中一定属于饱和溶液的是A(填序号),烧杯①中溶解的溶质是乙(填甲或乙);
(2)20℃时140g甲的饱和溶液稀释成10%的溶液,需加水260g;
(3)下列有关说法不正确的是AB
A.上图中A中上层清液中溶质质量分数>B中溶液溶质质量分数
B.上图中B、C、D烧杯里的溶液都可能是饱和溶液
C.从甲、乙的饱和溶液中提纯乙可采用升温的方法
D.甲、乙的饱和溶液分别从40℃降温到20℃,得到的溶液中溶质质量分数相等.
分析 根据题目信息和溶解度曲线可知:甲固体物质的溶解度,是随温度升高而增大,而乙的溶解度随温度的升高而减少;图1中一定属于饱和溶液的是A,因为烧杯底部有固体;烧杯①中溶解的溶质是乙,因为在40℃时,甲的溶解度大于乙;20℃时140g甲的饱和溶液稀释成10%的溶液,溶质的质量不变;下列有关说法不正确的是:上图中A中上层清液中溶质质量分数>B中溶液溶质质量分数错误,因为在该温度下相等质量的B全部溶解,A有剩余;上图中B、C、D烧杯里的溶液都可能是饱和溶液错误,因为B一定不饱和;正确的有:从甲、乙的饱和溶液中提纯乙可采用升温的方法正确,甲、乙的饱和溶液分别从40℃降温到20℃,得到的溶液中溶质质量分数相等正确,因为都是相同质量的溶质溶解在相等的水中.
解答 解:(1)图1中一定属于饱和溶液的是A,因为烧杯底部有固体;烧杯①中溶解的溶质是乙,因为在40℃时,甲的溶解度大于乙;故答案为:A;乙;
(2)20℃时140g甲的饱和溶液稀释成10%的溶液,溶质的质量不变,设加水的质量为x,(140g+x)×10%=40g,x=260g;故答案为:260;
(3)下列有关说法不正确的是:上图中A中上层清液中溶质质量分数>B中溶液溶质质量分数错误,因为在该温度下相等质量的B全部溶解,A有剩余;上图中B、C、D烧杯里的溶液都可能是饱和溶液错误,因为B一定不饱和;正确的有:从甲、乙的饱和溶液中提纯乙可采用升温的方法正确,因为乙的溶解度随温度的升高而减少;甲、乙的饱和溶液分别从40℃降温到20℃,得到的溶液中溶质质量分数相等正确,因为都是相同质量的溶质溶解在相等的水中;故答案为:AB;
点评 本考点考查了溶解度曲线及其应用,通过溶解度曲线我们可以获得很多信息;还考查了有关溶液和溶质质量分数的计算,有关的计算要准确,本考点主要出现在选择题和填空题中.

 阅读快车系列答案
阅读快车系列答案| 选项 | 物质 | 杂质 | 除杂方法 |
| A | NaNO3 | Na2CO3 | 加足量稀盐酸,蒸发结晶 |
| B | Cu | Fe | 加足量的稀硫酸,过滤 |
| C | CO2 | CO | 通过灼热的CuO |
| D | CaO | CaCO3 | 高温煅烧 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 蒸发5g水有固体溶质析出 | B. | 加入少许硝酸钾晶体不溶 | ||
| C. | 把溶液降温至0℃有固体溶质析出 | D. | 升高温度能继续溶解晶体 |
| A. | 饱和溶液恒温蒸发部分溶剂后溶质的质量分数一定不变 | |
| B. | 同种溶质的饱和溶液一定比它的不饱和溶液溶质的质量分数大 | |
| C. | 饱和溶液转化为不饱和溶液溶液的质量一定增大 | |
| D. | 不饱和溶液转化为饱和溶液溶质的质量分数一定变大 |
| A. |  向100g10%的氢氧化钠溶液中逐滴加入100g10%稀盐酸 | |
| B. |  向盛有部分变质的NaOH的溶液的烧杯中滴加稀硫酸至过量 | |
| C. |  将t2℃时溶质质量分数都为10%的a、b、c三种物质的溶液降温到t1℃所得溶液的溶质质量分数还都是10% | |
| D. |  向一定量NaOH和BaCl2的混合溶液中滴加稀硫酸至过量 |
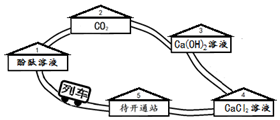 碳酸钠溶液搭乘列车畅游物质世界.如图所示.
碳酸钠溶液搭乘列车畅游物质世界.如图所示. 小明去采摘草莓.
小明去采摘草莓.