题目内容
3.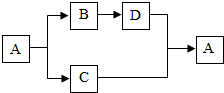 A〜D都是初中化学中的常见物质,且有如图所示的转化关系(反应条件、其他反应物及多余产物均已略去).请按要求填空:
A〜D都是初中化学中的常见物质,且有如图所示的转化关系(反应条件、其他反应物及多余产物均已略去).请按要求填空:(1)若A在常温下是一种无色液体,且D是CuO. 则:A的化学式为H2O,写出的化学反应方程式:H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O.
(2)若A在常温下是一种不溶于水的白色固体,且C是形成温室效应的主要气体之一.则:A的化学式为CaCO3,写出B→D的化学反应方程式:CaO+H2O=Ca(OH)2.
分析 (1)根据A在常温下是一种无色液体,A可能是水,D是氧化铜,水会分解成氢气和氧气,氧气会转化成氧化铜,氧化铜和氢气又会生成水,将各种物质代入转换关系进行验证即可;
(2)根据C是形成温室效应的主要气体之一,所以C是二氧化碳,A在常温下是一种不溶于水的白色固体,分解会生成二氧化碳,所以A可能是碳酸钙,B就是氧化钙,D是氢氧化钙,氢氧化钙和二氧化碳反应会生成碳酸钙,对各种物质进行验证即可;
解答 解:(1)A~D都是初中化学中的常见物质,A在常温下是一种无色液体,A可能是水,D是氧化铜,水会分解成氢气和氧气,氧气会转化成氧化铜,氧化铜和氢气又会生成水,经过验证各物质都满足转换关系,所以A是水,B会转化成氧化铜,B就是氧气,C就是氢气,氧化铜和氢气在加热的条件下生成水和铜,氢气发生的是还原反应,具有还原性,该反应由一种单质与一种化合物反应生成另一种单质和另一种化合物,符合置换反应的概念,属于置换反应,故答案为:H2O;H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O;
(2)C是形成温室效应的主要气体之一,所以C是二氧化碳,A在常温下是一种不溶于水的白色固体,分解会生成二氧化碳,所以A可能是碳酸钙,B就是氧化钙,D是氢氧化钙,氢氧化钙和二氧化碳反应会生成碳酸钙,经过验证各物质都满足转换关系,碳酸钙高温会分解成二氧化碳和氧化钙,所以B就是氧化钙,氧化钙和水反应会生成氢氧化钙,D就是氢氧化钙,氢氧化钙和二氧化碳会生成碳酸钙和水,故答案为:CaCO3; CaO+H2O=Ca(OH)2;
故答案为:
(1)H2O,H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O.(2)CaCO3,CaO+H2O=Ca(OH)2.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质题中的转换关系推导剩余的物质,最后进行验证即可.

 全优点练单元计划系列答案
全优点练单元计划系列答案| A. | 水泥 | B. | 塑料 | C. | 铝合金 | D. | 玻璃钢 |
| A. |  高锰酸钾溶液褪色 | B. |  红墨水如图移动 | ||
| C. | 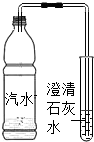 澄清石灰水变浑浊 | D. |  酚酞溶液不变色 |
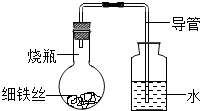 小明同学为了研究影响铁生锈的因素,进行了如下实验:
小明同学为了研究影响铁生锈的因素,进行了如下实验:在A、B、C、D四只烧瓶中分别放入干燥的细铁丝、浸过食盐水的细铁丝、浸过清水的细铁丝、食盐水及细铁丝(使细铁丝完全浸没在食盐水中)(四只烧瓶中细铁丝的质量均相同),然后装配成如图所示的四套装置,每隔0.5小时测量导管中水面上升的高度,结果如下表所示:
| 烧瓶号 | 时间/h 导管中水面上升高度/cm | 0 | 0.5 | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 |
| A瓶 | 盛干燥的细铁丝 | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
| B瓶 | 盛浸过食盐水的细铁丝 | 0 | 0.4 | 1.2 | 3.4 | 5.6 | 7.6 | 9.8 |
| C瓶 | 盛浸过清水的细铁丝 | 0 | 0 | 0 | 0.3 | 0.8 | 2.0 | 3.5 |
| D瓶 | 盛完全浸没在食盐水中的细铁丝 | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
(1)以上实验中,铁生锈的速率最大的是B(填烧瓶号).
(2)导管中水面上升的原因是烧瓶中的氧气参加反应,气体减少,压强降低.
(3)以上实验说明,影响铁生锈的因素是水和氧气,食盐能够促进铁生锈.
(4)为了防止钢铁锈蚀,人们常采用在其表面涂刷矿物油或镀上其他金属等覆盖保护膜的方法,这些方法的共同原理是隔绝氧气和水.
| A. | 红磷在空气中燃烧,生成浓重的白烟 | |
| B. | 二氧化碳通入氯化钙溶液中产生白色沉淀 | |
| C. | 用氢氧化钠固体与稀盐酸作用,验证得出中和反应放热 | |
| D. | 稀释浓硫酸时,将水慢慢倒入浓硫酸中,并不断搅拌散热 |
| A. | 干冰在空气中升华 | B. | 铁制品在空气中生锈 | ||
| C. | 浓硫酸在空气中变稀 | D. | 氢氧化钠在空气中变质 |
| A. | 溶液都是均一、稳定、无色的混合物 | |
| B. | 溶质以分子或离子的形式均匀分散在洛剂中 | |
| C. | 溶液中只能有一种溶质,溶质可以是固体、液体或气体 | |
| D. | 饱和溶液析出晶体后,溶质的质量分数一定减少 |

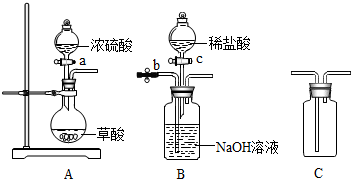 豆腐不可与菠菜一起煮,原因是菠菜含有丰富的草酸、草酸钠,豆腐中含有较多的硫酸钙等钙盐,相互反应生成草酸钙沉淀等物质.其中发生的反应属于D(填选项字母).
豆腐不可与菠菜一起煮,原因是菠菜含有丰富的草酸、草酸钠,豆腐中含有较多的硫酸钙等钙盐,相互反应生成草酸钙沉淀等物质.其中发生的反应属于D(填选项字母).