题目内容
5.用赤铁矿冶炼生铁的化学原理是Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2(用化学方程式表示),铁制品在潮湿的空气中生锈是由于铁与空气中的水蒸气和氧气反应生成铁锈,配制农药“波尔多液”时不用铁桶盛装硫酸铜溶液的原因是Fe+CuSO4=Cu+FeSO4(用化学方程式表示),常见金属铁、锌、铝的金属活动性顺序是铝>锌>铁.分析 工业上用一氧化碳还原氧化铁炼铁,主要是利用CO的还原性,在高温下和氧化铁反应生成铁和二氧化碳,写出反应的化学方程式即可.根据铁生锈的条件进行分析判断;
硫酸铜中的铜能被铁置换出来;根据金属活动性顺序来分析.
解答 解:工业上用一氧化碳还原氧化铁炼铁,主要是利用CO的还原性,在高温下和氧化铁反应生成铁和二氧化碳,反应的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;铁锈蚀的实质是铁与空气中的氧气、水蒸气等发生了化学变化,生成铁锈的主要成分是氧化铁;铁的活动性比铜强可以置换出铜,故答案为:Fe+CuSO4=Cu+FeSO4;在金属活动顺序中,铝排在锌的前面,锌排在铁的前面,故填:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;氧气;Fe+CuSO4=Cu+FeSO4;铝>锌>铁.
点评 本题考查了铁的冶炼、锈蚀,金属的活动性顺序以及化学方程式的书写,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15.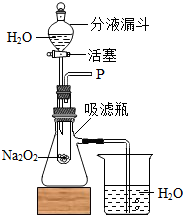 在学校的元旦联欢会上,某同学表演了‘水能生火’的魔术.他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.”小颖看到这段话后非常感兴趣,她和同学们一起对该问题进行了一系列的探究.
在学校的元旦联欢会上,某同学表演了‘水能生火’的魔术.他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.”小颖看到这段话后非常感兴趣,她和同学们一起对该问题进行了一系列的探究.
【提出问题】过氧化钠与水反应生成了什么物质?为什么脱脂棉会燃烧?
【猜想】①可能有一种气体和另一种物质生成②反应过程中可能有能量变化
【设计装置]如图所示
【实验探究】
实验一:探究反应后生成的气体是什么?
(1)打开如图装置中分液漏斗的活塞,控制滴加水的速度,观察到试管内有气泡产生,用带火星的木条靠近P处,木条复燃.说明生成的气体是氧气.
(2)实验中,还观察到伸入烧杯中的导管口有气泡冒出,请解释产生该现象的原因:反应放出热量,吸滤瓶中的空气受热膨胀,从导管逸出.
实验二:探究反应后生成的另一种物质是什么?
(1)小明猜想另一种物质是Na2CO3,小军认为不可能.为了证实小军的看法,请你设计一个证明Na2CO3不存在的实验:
(2)小军取反应后所得的溶液于试管中,滴入无色酚酞试液,发现试管中的溶液变成红色,说明反应后所得的溶液呈碱性.
【表达】小军根据实验探究的结果,写出了过氧化钠和水反应的化学方程式为2Na2O2+2H2O═4NaOH+O2↑.
 在学校的元旦联欢会上,某同学表演了‘水能生火’的魔术.他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.”小颖看到这段话后非常感兴趣,她和同学们一起对该问题进行了一系列的探究.
在学校的元旦联欢会上,某同学表演了‘水能生火’的魔术.他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.”小颖看到这段话后非常感兴趣,她和同学们一起对该问题进行了一系列的探究.【提出问题】过氧化钠与水反应生成了什么物质?为什么脱脂棉会燃烧?
【猜想】①可能有一种气体和另一种物质生成②反应过程中可能有能量变化
【设计装置]如图所示
【实验探究】
实验一:探究反应后生成的气体是什么?
(1)打开如图装置中分液漏斗的活塞,控制滴加水的速度,观察到试管内有气泡产生,用带火星的木条靠近P处,木条复燃.说明生成的气体是氧气.
(2)实验中,还观察到伸入烧杯中的导管口有气泡冒出,请解释产生该现象的原因:反应放出热量,吸滤瓶中的空气受热膨胀,从导管逸出.
实验二:探究反应后生成的另一种物质是什么?
(1)小明猜想另一种物质是Na2CO3,小军认为不可能.为了证实小军的看法,请你设计一个证明Na2CO3不存在的实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 取适量反应后的溶液于一试管中,向试管中滴加适量的稀盐酸 | 不产生气泡 | 生成物中没有Na2CO3 |
【表达】小军根据实验探究的结果,写出了过氧化钠和水反应的化学方程式为2Na2O2+2H2O═4NaOH+O2↑.
13.能直接在酒精灯火焰上加热的玻璃仪器是( )
| A. | 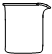 | B. | 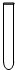 | C. | 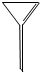 | D. |  |
20.下列叙述正确的是( )
| A. | 油脂和糖类物质能为人体提供能量 | |
| B. | 碳、氢、氧三种元素只能形成一种化合物 | |
| C. | 尼龙、涤纶和棉花都是合成纤维 | |
| D. | 塑料焚烧是消除“白色污染”的最佳方法 |
10.取某钢样粉末28.12g(假设只含Fe和C),在氧气流中充分反应,将产生的气体通入足量的澄清石灰水中,得到1g白色沉淀.
①计算此钢样粉末中铁和碳的质量之比.
②再取三份不同质量的钢样粉末分别加到50g质量分数相同的稀H2SO4中,充分反应后,测得的实验数据如下表所示:(标准状况下,2gH2的体积为22.4L)
请根据表中数据计算稀硫酸中H2SO4的质量分数.
③若在实验Ⅱ中继续加入mg钢样粉末,计算反应结束后剩余的固体质量为多少?(用含m的代数式表示)
①计算此钢样粉末中铁和碳的质量之比.
②再取三份不同质量的钢样粉末分别加到50g质量分数相同的稀H2SO4中,充分反应后,测得的实验数据如下表所示:(标准状况下,2gH2的体积为22.4L)
| 实验序号 | Ⅰ | Ⅱ | Ⅲ |
| 加入钢样粉末的质量/g | 2.812 | 5.624 | 8.436 |
| 生成气体的体积/L(标准状况) | 1.120 | 2.240 | 2.800 |
③若在实验Ⅱ中继续加入mg钢样粉末,计算反应结束后剩余的固体质量为多少?(用含m的代数式表示)