题目内容
9. 在盛有稀硫酸的烧杯中,漂浮着一木块,如图所示.
在盛有稀硫酸的烧杯中,漂浮着一木块,如图所示.如果往烧杯中中入少量某种固体物质后,木块浸没在水中的体积变大,加入固体物质可能是Ba(OH)2(写化学式),理由是稀硫酸和氢氧化钡反应生成硫酸钡沉淀和水,反应后,溶液的密度变小,而木块所受的浮力不变,由F=ρgV排知,木块排开水的体积将变大.
分析 氢氧化钡和稀硫酸反应生成白色沉淀硫酸钡和水;
漂浮在液体中的木块受到的浮力大于木块的重力.
解答 解:如果往烧杯中中入少量某种固体物质后,木块浸没在水中的体积变大,加入固体物质可能是Ba(OH)2,理由是稀硫酸和氢氧化钡反应生成硫酸钡沉淀和水,反应后,溶液的密度变小,而木块所受的浮力不变,由F=ρgV排知,木块排开水的体积将变大.
故填:Ba(OH)2;稀硫酸和氢氧化钡反应生成硫酸钡沉淀和水,反应后,溶液的密度变小,而木块所受的浮力不变,由F=ρgV排知,木块排开水的体积将变大.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案
相关题目
5.某温度时,A物质的溶解度是25g,则A的饱和溶液中溶质的质量分数是( )
| A. | 20% | B. | 25% | C. | 40% | D. | 50% |
6.氢气还原氧化铜实验得到的固体粉末为氧化铜和铜的混合物.某化学兴趣小组的同学对该粉末中单质铜的含量进行测定;取10g粉末样品置于烧杯中,向其中分5此加入相同溶质质量分数的稀硫酸,使之充分反应.每次所用稀硫酸的质量及剩余固体的质量记录如下:
实验所得数据见下表,请你分析并进行有关计算:
(1)表格中m=9.2;
(2)样品中单质铜的质量分数为71%;
(3)加入的稀硫酸溶质质量分数是多少?(写出计算过程)
实验所得数据见下表,请你分析并进行有关计算:
| 加入稀硫酸的质量(g) | 剩余固体质量(克) | |
| 第1次 | 10 | m |
| 第2次 | 10 | 8.4 |
| 第3次 | 10 | 7.6 |
| 第4次 | 10 | 7.1 |
| 第5次 | 10 | 7.1 |
(2)样品中单质铜的质量分数为71%;
(3)加入的稀硫酸溶质质量分数是多少?(写出计算过程)
17.某同学用一定溶质质量分数的稀硫酸做“氧化铜+硫酸→硫酸铜+水”的实验,其5次实验结果如表所示,根据实验结果填写下列空格:
(1)哪几次反应氧化铜有剩余?3、5
(2)表中x的值是16
(3)求硫酸溶液中溶质的质量分数.
| 实验次数 | 氧化铜/g | 硫酸溶液/g | 硫酸铜/g |
| 1 | 2.0 | 120 | 4.0 |
| 2 | 4.0 | 120 | 8.0 |
| 3 | 6.0 | 120 | 9.6 |
| 4 | 8.0 | 200 | 16 |
| 5 | 10.0 | 200 | X |
(2)表中x的值是16
(3)求硫酸溶液中溶质的质量分数.
4.下列实验操作错误的是( )
| A. | 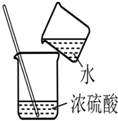 稀释浓硫酸 | B. | 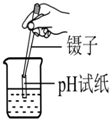 测定溶液pH值 | ||
| C. | 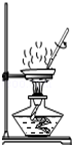 蒸发食盐水 | D. | 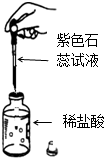 检验稀盐酸的酸碱性 |
14.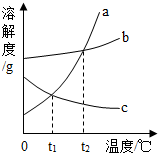 溶解度曲线是物质溶解性的直观体现.如图是a、b、c三种物质的溶解度曲线,下列说法正确的是( )
溶解度曲线是物质溶解性的直观体现.如图是a、b、c三种物质的溶解度曲线,下列说法正确的是( )
 溶解度曲线是物质溶解性的直观体现.如图是a、b、c三种物质的溶解度曲线,下列说法正确的是( )
溶解度曲线是物质溶解性的直观体现.如图是a、b、c三种物质的溶解度曲线,下列说法正确的是( )| A. | b物质可能是熟石灰 | |
| B. | a物质的溶解度大于b物质 | |
| C. | 使c物质结晶析出可以采用降温的方法 | |
| D. | t2时a、b两种物质饱和溶液的溶质质量分数相等 |
1.下列图象不能正确反映其对应操作中各量变化关系的是( )


| A. | 向等质量的锌片、铁片分别加入足量的等质量分数的稀硫酸 | |
| B. | 电解水 | |
| C. | 向氯化铁和盐酸的混合溶液中加入过量的氢氧化钠溶液 | |
| D. | 用两份等质量的氯酸钾分别制取氧气 |
18.下列“家庭小实验”能成功的是:①用铅笔芯的粉末使锁的开启变灵活;②在煤炉上放一盆水来防止煤气中毒;③用浓硫酸制作“叶脉书签”;④用木炭除去水中的异味和色素;⑤用食醋除去热水瓶胆中的水垢.( )
| A. | ①④⑤ | B. | ①②④ | C. | ②④⑤ | D. | ①③⑤ |
19.下列实验操作正确的是( )
| A. | 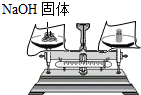 称量氢氧化钠 | B. | 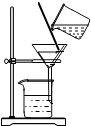 过滤 | ||
| C. | 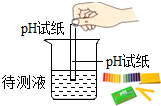 测定溶液pH | D. |  稀释浓硫酸 |