题目内容
16.甲烷是天然气的主要成分,其化学式为CH4,下列有关说法正确的是( )| A. | 甲烷中的C、H元素的质量比为1:4 | |
| B. | 甲烷分子是由1个碳元素和4个氢元素组成 | |
| C. | 甲烷分子中碳的原子结构示意图为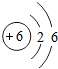 | |
| D. | 甲烷是最简单的有机物 |
分析 A.根据化合物中元素的质量比计算方法来分析;
B.根据元素的规定来分析;
C.根据碳原子结构来分析;
D.根据结构最简单的有机物来分析.
解答 解:A.甲烷中碳、氢元素质量比为:12:(1×4)=3:1.故错误;
B.元素是个宏观概念,只讲种类、不讲个数,故错误;
C.在原子中,核内质子数=核外电子数,故错误;
D.甲烷是结构最简单的有机物,故正确.
故选D.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目
6.空气质量事关人类生存质量,PM2.5也是空气中污染物之一,要加强监测,采取措施,确保指数达标,关于PM2.5产生的原因分析不正确的是( )
| A. | 火力发电 | B. | 焚烧垃圾 | C. | 建筑粉尘 | D. | 白色污染 |
7.某工厂利用熟石灰除去废液中残余的盐酸,使废液呈中性而达到排放标准.某校化学兴趣小组成员取处理后的废液样品进行检测.
【提出问题】样品中的溶质是什么?
【作出猜想】猜想一:只有CaCI2;
猜想二:可能是CaCl2和Ca(OH)2
猜想三:可能是CaCl2和HCl.
【查阅资料】氯化钙溶液呈中性.
【进行实验】甲、乙两位同学用不同类别的试剂进行实验,得到同样结论.
【反思与评价】
(1)用熟石灰除去废液中残余盐酸的化学方程式是Ca(OH)2+2HCl=CaCl2+2H2O.
(2)为避免这种不符合排放标准的结果出现,你认为处理废液中残余盐酸时,可以使用过量的石灰石.
【提出问题】样品中的溶质是什么?
【作出猜想】猜想一:只有CaCI2;
猜想二:可能是CaCl2和Ca(OH)2
猜想三:可能是CaCl2和HCl.
【查阅资料】氯化钙溶液呈中性.
【进行实验】甲、乙两位同学用不同类别的试剂进行实验,得到同样结论.
| 实验步骤 | 实验现象 | 实验结论 | |
| 甲 | 取少量样品于试管中,滴入几滴无色酚酞溶液 | 溶液由无色变红色 | 猜想二正确 |
| 乙 | 取少量样品于试管中,加入硫酸铜溶液(或通入二氧化碳) | 有蓝色沉淀产生(或产生白色沉淀) |
(1)用熟石灰除去废液中残余盐酸的化学方程式是Ca(OH)2+2HCl=CaCl2+2H2O.
(2)为避免这种不符合排放标准的结果出现,你认为处理废液中残余盐酸时,可以使用过量的石灰石.
4.现有实验操作后某废液缸中的一杯无色溶液.关于该溶液中所含溶质,有如下几种猜测,其中合理的( )
| A. | H2SO4、KOH、NaCl | B. | KNO3、NaCl、CuSO4 | ||
| C. | AgNO3、NaCl、HCl | D. | H2SO4、Na2SO4、KNO3 |
8.下列说法正确的是( )
| A. | 碘易溶于水而难溶于汽油,高锰酸钾易溶于汽油,可用水区分碘和高锰酸钾 | |
| B. | 硫酸铵易溶于水,长期施用会使土壤酸化,遇熟石灰能放出氨气 | |
| C. | 气体溶解度是指在1标准大气压下和0℃,1体积水里达饱和时溶解的气体体积 | |
| D. | 18K黄金主要成分是金、铜、锌,具有光泽好、耐磨、易加工性能,常做金饰品 |
15.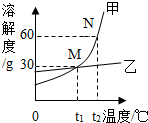 甲、乙两种不含结晶水的固体物质的溶解度曲线如图,下列说法中正确的是( )
甲、乙两种不含结晶水的固体物质的溶解度曲线如图,下列说法中正确的是( )
 甲、乙两种不含结晶水的固体物质的溶解度曲线如图,下列说法中正确的是( )
甲、乙两种不含结晶水的固体物质的溶解度曲线如图,下列说法中正确的是( )| A. | t2℃时,向50g水中加入30g乙可得到80g乙的饱和溶液 | |
| B. | 在t1℃时,两种物质的饱和溶液中溶质的质量相等 | |
| C. | 当甲中混有少量乙时,通常可采用蒸发结晶的方法提纯甲 | |
| D. | t2℃时等质量的两种物质的饱和溶液,降温到t1℃时所得甲、乙饱和溶液的质量一定不相等 |
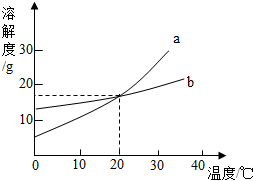 如图是a、b两种固体物质的溶解度曲线.
如图是a、b两种固体物质的溶解度曲线.