题目内容
3.可能由CO、H2、O2、N2混合而成的某气体,通过盛有加热氧化铜玻璃管时,氧化铜逐渐被还原,由此可判断原气体中肯定没有氧气;将反应后的气体导出通入石灰水中,石灰水变浑浊,由此可判断原气体中肯定含有一氧化碳.分析 根据CO、H2具有还原性,能与灼热的氧化铜反应,二氧化碳能使澄清的石灰水变浑浊,进行分析解答.
解答 解:可能由CO、H2、O2、N2混合而成的某气体,通过盛有加热氧化铜玻璃管时,氧化铜逐渐被还原,说明混合气体中含有还原性的气体,可能含有氢气或一氧化碳,一定不含氧气(氧气能与生成的铜反应再次生成氧化铜);将反应后的气体导出通入石灰水中,石灰水变浑浊,说明生成了二氧化碳,则原气体中肯定含有一氧化碳.
故答案为:氧气;一氧化碳.
点评 本题难度不大,熟练掌握常见气体的性质、检验方法并能灵活运用是正确解答此类题的关键.

练习册系列答案
相关题目
14.下列物质属于氧化物的是( )
| A. | 水蒸气 | B. | 空气 | C. | 液氧 | D. | 氯酸钾 |
11.尿素CO(NH2)2中N元素的质量分数也叫含氮量,其含氮量为( )
| A. | 32.5% | B. | 46.7% | C. | 55.0% | D. | 94.2% |
18.决定元素种类的是( )
| A. | 电子数 | B. | 质子数 | C. | 中子数 | D. | 原子核 |
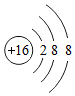 表示的是S2-(填微粒符号),其核电荷数为16.
表示的是S2-(填微粒符号),其核电荷数为16.
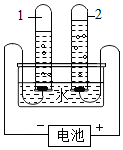 (1)根据物质初步分类的知识,在①双氧水的溶液;②液态氧;③四氧化三铁;④氯酸钾;⑤二氧化碳;⑥自来水;⑦铜粉中属于混合物的是①⑥(填序号,下同);属于纯净物的是②③④⑤⑦.属于单质的是②⑦;属于化合物的是③④⑤;属于氧化物的是③⑤.
(1)根据物质初步分类的知识,在①双氧水的溶液;②液态氧;③四氧化三铁;④氯酸钾;⑤二氧化碳;⑥自来水;⑦铜粉中属于混合物的是①⑥(填序号,下同);属于纯净物的是②③④⑤⑦.属于单质的是②⑦;属于化合物的是③④⑤;属于氧化物的是③⑤.