题目内容
15.某种元素化合价在化学反应前后发生了变化,则该反应为氧化还原反应.据此可判断下列化学反应属于氧化还原反应的有( )| A. | ZnO+H2SO4═ZnSO4+H2O | B. | Fe2O3+3CO $\frac{\underline{\;高温\;}}{\;}$ 2Fe+3CO2 | ||
| C. | Na2CO3+2HCl═2NaCl+H2O+CO2↑ | D. | CaCO3 $\frac{\underline{\;高温\;}}{\;}$ CaO+CO2↑ |
分析 根据题干提供的信息进行分析,元素化合价在化学反应前后发生了变化,则该反应为氧化还原反应,据此解答.
解答 A.ZnO+H2SO4=ZnSO4+H2O,该反应前后元素的化合价没有发生改变,不是氧化还原反应,故错误;
B.Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,该反应中,反应前铁元素的化合价是+3,反应后铁元素的化合价为0,反应前碳元素的化合价是+2,反应后碳元素的化合价是+4,元素的化合价发生改变,属于氧化还原反应,故正确;
C.Na2CO3+2HCl═2NaCl+H2O+CO2↑,该反应的前后各元素化合价不变,故不属于氧化还原反应,故错误;
D.CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑,该反应前后元素的化合价没有发生改变,不是氧化还原反应,故错误.
故选B.
点评 解答本题要充分理解氧化还原反应的含义是某种元素化合价在化学反应前后发生了变化,只有这样才能对相关方面的反应做出正确的判断.

练习册系列答案
相关题目
3.在AgNO3和Zn(NO3)2的混合溶液中,加入一定量的铁粉充分反应后,过滤,洗涤,将滤渣放入盐酸中有气泡产生,则滤渣成分的组成是( )
| A. | Fe Ag | B. | Fe Zn | C. | Zn Ag | D. | Zn Ag Fe |
10.下列图示实验的操作中,正确的是( )
| A. | 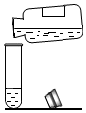 倾倒液体 | B. | 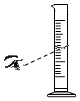 读取体积 | C. | 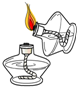 点燃酒精灯 | D. | 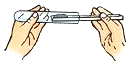 装入固体粉末 |
20.下列物质属于纯净物的是( )
| A. | 硬铝 | B. | 啤酒 | C. | 水银 | D. | 河水 |
7.某同学对化学知识的归纳正确的是( )
| A. | pH>7的溶液一定是碱的溶液 | |
| B. | 同种元素组成的物质一定是单质 | |
| C. | 生成盐和水的反应一定是复分解反应 | |
| D. | 能分解生成氧气的物质一定含有氧元素 |
4.地壳中含量最高的金属元素是( )
| A. | Ca | B. | Si | C. | Al | D. | O |

 室温下,将稀盐酸慢慢滴入装有氢氧化钠溶液的烧杯中,利用温度计测出烧杯中溶液的温度,溶液温度随加入盐酸的质量而变化的曲线如图所示:
室温下,将稀盐酸慢慢滴入装有氢氧化钠溶液的烧杯中,利用温度计测出烧杯中溶液的温度,溶液温度随加入盐酸的质量而变化的曲线如图所示: 如图,烧杯中放入NaOH溶液,将透明装置密封后放入水浴中,水浴温度始终维持在25℃,关闭阀门,并置于暗处,1小时后可观察到红墨水滴向左(选填“左”、“右”)移动,请你用科学原理解释其原因植物在黑暗下呼吸作用,吸收装置中的氧气,同时呼出CO2,释放的CO2被NaOH溶液吸收,所以密闭装置中的气体量变少,气压也变小,小于外界大气压,在外界大气压的作用下,红墨水向左移动.(实验中植物蒸腾作用、空气湿度、微生物等因素的影响忽略不计).
如图,烧杯中放入NaOH溶液,将透明装置密封后放入水浴中,水浴温度始终维持在25℃,关闭阀门,并置于暗处,1小时后可观察到红墨水滴向左(选填“左”、“右”)移动,请你用科学原理解释其原因植物在黑暗下呼吸作用,吸收装置中的氧气,同时呼出CO2,释放的CO2被NaOH溶液吸收,所以密闭装置中的气体量变少,气压也变小,小于外界大气压,在外界大气压的作用下,红墨水向左移动.(实验中植物蒸腾作用、空气湿度、微生物等因素的影响忽略不计).