题目内容
5.将含泥沙的粗盐提纯,并用制得的精盐配制80g10%的食盐溶液.下列说法错误的是( )| A. | 配制溶液的步骤是:计算、称量、溶解、转移装瓶、贴标签 | |
| B. | 配制时需用的主要仪器有:天平、药匙、量筒、胶头滴管、烧杯、玻璃棒 | |
| C. | 过滤操作时,搅拌漏斗中的液体,可以加快过滤的速度 | |
| D. | 蒸发滤液时,不断用玻璃棒搅拌,防止液体溅出 |
分析 A、根据配制溶质质量分数一定的溶液的基本步骤进行分析判断.
B、根据配制溶质质量分数一定的溶液的步骤分析解答需要的仪器,进行分析判断.
C、过滤液体时,注意“一贴、二低、三靠”的原则.
D、根据蒸发操作的注意事项进行分析判断.
解答 解:A、配制80g10%的食盐溶液,首先计算配制溶液所需食盐和水的质量,再称量所需的食盐和量取水,最后进行溶解、转移装瓶、贴标签,故选项说法正确.
B、药匙用于取用食盐,托盘天平用于称取固体食盐,量筒与胶头滴管用于准确量取水,烧杯用于完成溶解操作、玻璃棒用于溶解时的搅拌,故选项说法正确.
C、过滤操作时,不能搅拌漏斗中的液体,以防止损坏滤纸,故选项说法错误.
D、蒸发滤液时,不断用玻璃棒搅拌,以防止液体受热不均匀溅出,故选项说法正确.
故选:C.
点评 本题难度不大,掌握配制溶质质量分数一定的溶液的基本步骤、所需仪器、过滤与蒸发操作的注意事项等是正确解答本题的关键.

练习册系列答案
 初中学业考试导与练系列答案
初中学业考试导与练系列答案
相关题目
7.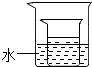 下面的表格中列出了氯化铵在不同温度下的溶解度:
下面的表格中列出了氯化铵在不同温度下的溶解度:
(1)从表中可得到的一条信息是氯化铵的溶解度随温度升高而增大;
(2)20℃时,向50g水中加入20g氯化铵,形成氯化铵的饱和(填“饱和”或“不饱和”)溶液,将其温度升高至60℃时,所得溶液的质量为150克;
(3)将(2)中所得的60℃时的氯化铵溶液放入如图所示的小烧杯中,在大烧杯的水中加入下列物质,能够使小烧杯中有固体析出的是AC(填字母序号);
A.冰 B.氯化钠 C.硝酸铵 D.氧化钙
(4)某同学欲配制20℃时20%的氯化铵溶液500g,需要氯化铵的质量100g.他在量取水时俯视读数,在其他操作都无误的情况下,他配制的溶液的溶质质量分数将偏大(填“偏大”或“偏小”).
 下面的表格中列出了氯化铵在不同温度下的溶解度:
下面的表格中列出了氯化铵在不同温度下的溶解度:| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| 溶解度/g | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 | 60.2 | 65.6 |
(2)20℃时,向50g水中加入20g氯化铵,形成氯化铵的饱和(填“饱和”或“不饱和”)溶液,将其温度升高至60℃时,所得溶液的质量为150克;
(3)将(2)中所得的60℃时的氯化铵溶液放入如图所示的小烧杯中,在大烧杯的水中加入下列物质,能够使小烧杯中有固体析出的是AC(填字母序号);
A.冰 B.氯化钠 C.硝酸铵 D.氧化钙
(4)某同学欲配制20℃时20%的氯化铵溶液500g,需要氯化铵的质量100g.他在量取水时俯视读数,在其他操作都无误的情况下,他配制的溶液的溶质质量分数将偏大(填“偏大”或“偏小”).
8.下列各组物质混合后,如其中的酸过量时,有沉淀生成的是( )
| A. | 氯化钾、碳酸钠、硫酸 | B. | 硫酸铜、氢氧化钠、盐酸 | ||
| C. | 氯化钡、硝酸银、硝酸 | D. | 氯化铁、氢氧化锌、硝酸 |
20.20°C时100g某硝酸钾溶液,经过以下变化,恢复到20°C,最终析出晶体的质量是( )


| A. | 小于3克 | B. | 等于3克 | C. | 大于3克 | D. | 大于等于3克 |
15.下列各符号中数字“2”表示的意义不正确的是( )
| A. | N2:一个氮分子由两个氮原子构成 | |
| B. | Fe2+:一个铁离子带两个单位的正电荷 | |
| C. | 2Hg:二个汞原子 | |
| D. | 2NO3-:二个硝酸根离子 |

 电解法制铝的尾气处理工艺不仅能消除有害气体氟化氢(HF),还能实现物质的循环利用.主要物质转化关系如图所示:
电解法制铝的尾气处理工艺不仅能消除有害气体氟化氢(HF),还能实现物质的循环利用.主要物质转化关系如图所示: