题目内容
11.15g不纯锌粒与100g稀硫酸充分反应得到0.4g氢气,(无晶体析出)求:(1)锌粒的纯度?
(2)稀硫酸溶液的溶质质量分数?
(3)生成硫酸锌溶液的溶质质量分数?
分析 锌和稀硫酸反应生成硫酸锌和氢气,根据氢气质量可以计算锌的质量、反应的硫酸质量和反应生成的硫酸锌质量,进一步可以计算锌粒的纯度、稀硫酸溶液的溶质质量分数、生成硫酸锌溶液的溶质质量分数.
解答 解:(1)设锌的质量为x,硫酸质量为y,生成硫酸锌质量为z,
Zn+H2SO4═ZnSO4+H2↑,
65 98 161 2
x y z 0.4g
$\frac{65}{x}$=$\frac{98}{y}$=$\frac{161}{z}$=$\frac{2}{0.4g}$,
x=13g,y=19.6g,z=32.2g,
锌粒的纯度为:$\frac{13g}{15g}$×100%=86.7%,
(2)稀硫酸溶液的溶质质量分数为:$\frac{19.6g}{100g}$×100%=19.6%,
(3)生成硫酸锌溶液的溶质质量分数为:$\frac{32.2g}{13g+100g-0.4g}$×100%=28.6%,
答:锌的纯度是86.7%,稀硫酸质量分数是19.6%,硫酸锌溶液中硫酸锌的质量分数是28.6%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
2.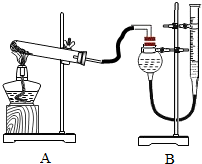 实验室常用氯酸钾与二氧化锰的混合物来制取氧气,二氧化锰能加快氯酸钾的分解.现设计实验证明氧化铜也能加快氯酸钾的分解,并与二氧化锰的催化效果进行比较(即比较反应的快慢),用如图装置进行实验.实验时均以生成25mL气体为准,其他可能影响实验的因素已忽略.相关数据见下表
实验室常用氯酸钾与二氧化锰的混合物来制取氧气,二氧化锰能加快氯酸钾的分解.现设计实验证明氧化铜也能加快氯酸钾的分解,并与二氧化锰的催化效果进行比较(即比较反应的快慢),用如图装置进行实验.实验时均以生成25mL气体为准,其他可能影响实验的因素已忽略.相关数据见下表
回答下列问题:
(1)上述实验中的“待测数据”指生成25mL气体所需的时间;
(2)本实验装置图中量气装置B由球形干燥管、乳胶管和50mL带刻度玻璃管改造后组装而成.此处所用液体通常选择A(填字母编号)
A、水 B、浓硫酸 C、双氧水 D、无水酒精
(3)若要证明实验②中球形干燥管内收集的气体是O2,可待气体收集结束后.先调整B装置左右液面相平,再用弹簧夹夹住B中乳胶管,拔去干燥管上单孔橡皮塞,伸入带火星的木条,观察现象.
(4)为探究CuO在实验②中是否起催化作用,除与实验①比较外,还需补做如下实验(无需写出具体操作):证明CuO的质量没有改变或CuO的化学性质没有改变.
 实验室常用氯酸钾与二氧化锰的混合物来制取氧气,二氧化锰能加快氯酸钾的分解.现设计实验证明氧化铜也能加快氯酸钾的分解,并与二氧化锰的催化效果进行比较(即比较反应的快慢),用如图装置进行实验.实验时均以生成25mL气体为准,其他可能影响实验的因素已忽略.相关数据见下表
实验室常用氯酸钾与二氧化锰的混合物来制取氧气,二氧化锰能加快氯酸钾的分解.现设计实验证明氧化铜也能加快氯酸钾的分解,并与二氧化锰的催化效果进行比较(即比较反应的快慢),用如图装置进行实验.实验时均以生成25mL气体为准,其他可能影响实验的因素已忽略.相关数据见下表| 实验序号 | KClO3质量 | 催化剂 | 待测数据 |
| ① | 1.2g | 无其他物质 | |
| ② | 1.2g | CuO0.5g | |
| ③ | 1.2g | MnO20.5g |
(1)上述实验中的“待测数据”指生成25mL气体所需的时间;
(2)本实验装置图中量气装置B由球形干燥管、乳胶管和50mL带刻度玻璃管改造后组装而成.此处所用液体通常选择A(填字母编号)
A、水 B、浓硫酸 C、双氧水 D、无水酒精
(3)若要证明实验②中球形干燥管内收集的气体是O2,可待气体收集结束后.先调整B装置左右液面相平,再用弹簧夹夹住B中乳胶管,拔去干燥管上单孔橡皮塞,伸入带火星的木条,观察现象.
(4)为探究CuO在实验②中是否起催化作用,除与实验①比较外,还需补做如下实验(无需写出具体操作):证明CuO的质量没有改变或CuO的化学性质没有改变.
19.上海染色馒头事件曾一度引起人们的恐慌,该公司在馒头中添加了一种叫做柠檬黄的物质,食用染色馒头会出现一些过敏反应,柠檬黄的化学式为C16H9N4O9S2Na3,下列相关叙述正确的是( )
| A. | 柠檬黄是由七种元素组成的 | B. | 柠檬黄是混合物 | ||
| C. | 柠檬黄的相对分子质量为534 | D. | 氢氧元素质量比为1:1 |
6.据报道,目前有些中小学生喜欢使用涂改液,经实验证明涂改液中含有很多挥发性有害物质,吸入后易引起慢性中毒而头晕、头痛,严重者抽搐、呼吸困难,二氯甲烷就是其中一种.下面关于二氯甲烷(CH2Cl2)的几种叙述中,正确的是( )
| A. | 它是由碳、氢、氯三种元素组成的化合物 | |
| B. | 它是由氯气和甲烷组成的混合物 | |
| C. | 它的分子中碳、氢、氯元素的原子个数比是6:1:35.5 | |
| D. | 它是一种氧化物 |
3.今年潍坊出现严重干旱,爱护水资源,节约用水,防止水污染应成为我们的自觉行为,下列有关水资源利用合理的是( )
| A. | 为不浪费水,工业废水直接灌溉庄稼 | |
| B. | 农业生产中使用浸灌方式灌溉庄稼,水分能充分吸收,有利节约用水 | |
| C. | 大量开采地下水以满足社会对水的需求 | |
| D. | 使用无磷洗衣粉有利于保护水资源 |
1.在硝酸中混有少量盐酸,加入下列各物质中的哪一种就可以将盐酸除去( )
| A. | 硝酸银溶液 | B. | 汽油 | C. | 肥皂水 | D. | 烧碱溶液 |
