题目内容
【题目】氢氧化钠和氢氧化钙是两种常见的碱.李红同学将两种碱的溶液分别装入试管A,B中,并进行了如图所示的三组实验. 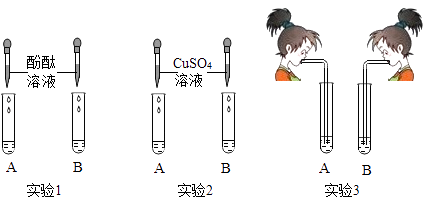
(1)实验l 中,两支试管的溶液都变成 .
(2)实验2中,若B 盛装的是NaOH 溶液,发生反应的化学方程式为: .
(3)实验3中,李红同学向两支试管吹气,A 中有白色沉淀生成,发生反应的化学方程式为: .
B 中无现象,为了探究吹气后B 中溶质的成分,李红进行了如下探究.
【提出猜想】:
猜想1:溶质只有氢氧化钠
猜想2:溶质只有碳酸钠
猜想3: .
【实验和结论】:
实验 | 实验现象 | 结论 |
取B 中少量溶液,加人澄清石灰水至不再 | 产生白色沉淀 | 猜想3成立 |
【反思与评价】:
同学们相互讨论后,李红得出的结论(填“正确”或“不正确”),其原因是猜想(填数字)也会产生相同的现象.
【答案】
(1)红
(2)2NaOH+CuSO4═Cu(OH)2↓+Na2SO4
(3)Ca(OH)2+CO2═CaCO3↓+H2O;溶质有氢氧化钠和碳酸钠;不正确;2
【解析】解:(1)实验1中,两支试管的溶液都显碱性,都能够使酚酞试液变红色.(2)实验2中,若B盛装的是NaOH溶液,氢氧化钠和硫酸铜反应生成氢氧化铜沉淀和硫酸钠,发生反应的化学方程式为:2NaOH+CuSO4═Cu(OH)2↓+Na2SO4;(3)实验3中,向两支试管吹气,A中有白色沉淀生成,说明A中是澄清石灰水,澄清石灰水中的氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水,发生反应的化学方程式为:Ca(OH)2+CO2═CaCO3↓+H2O;【提出猜想】:猜想1:溶质只有氢氧化钠猜想2:溶质只有碳酸钠
猜想3:溶质有氢氧化钠和碳酸钠【反思与评价】:李红得出的结论不正确,是因为猜想2中也会产生相同的现象,这是因为如果溶质只有碳酸钠,则碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,氢氧化钠溶液能使酚酞试液变红色,如果要验证“猜想3成立”,必需更换试剂,将氢氧化钙溶液换成氯化钙溶液,这是因为氯化钙和碳酸钠反应生成碳酸钙沉淀和氯化钠,氯化钠溶液显中性,不能使酚酞试液变色.答案:(1)红;(2)2NaOH+CuSO4═Cu(OH)2↓+Na2SO4;(3)Ca(OH)2+CO2═CaCO3↓+H2O;【提出猜想】:溶质有氢氧化钠和碳酸钠;【反思与评价】:不正确;2.
(1)显碱性的溶液能使酚酞试液变红色;(2)氢氧化钠和硫酸铜反应生成蓝色沉淀氢氧化铜和硫酸钠;(3)氢氧化钙能和二氧化碳反应生成白色沉淀碳酸钙和水,氢氧化钠能和二氧化碳反应生成碳酸钠和水;氢氧化钙能和碳酸钠反应生成白色沉淀碳酸钙和氢氧化钠.

 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案