题目内容
 碳酸氢钠是一种重要的盐类物质,在生活中用途广泛.小滨同学设计了实验,以探究碳酸氢钠的化学性质.
碳酸氢钠是一种重要的盐类物质,在生活中用途广泛.小滨同学设计了实验,以探究碳酸氢钠的化学性质.【探究实验1】碳酸氢钠溶液的酸碱性
【实验方案】取少量该固体加入试管中,加适量水溶解,再滴入几滴酚酞实验,震荡.
现象:溶液变成浅红色.由此得出结论
【探究实验2】能与酸反应
【实验方案】取少量该固体加入试管中,滴加稀盐酸,现象为
【探究实验3】碳酸氢钠的热稳定性
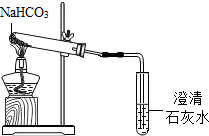
【实验方案】用如图所示装置进行实验
现象:充分加热后,大试管口有水珠出现,管底有白色固体残留,小试管中澄清石灰石变浑浊.
结论:碳酸氢钠受热能生成二氧化碳、水和一种白色固体.
验证:(1)请你帮小滨设计实验,证明试管中留下的白色固体是Na2CO3,而不是NaOH(所选试剂不能用酸).
步骤
(2)写出碳酸氢钠受热分解的化学方程式
【拓展应用】试说出碳酸氢钠在日常生活中的一种用途
考点:盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:常见的盐 化学肥料
分析:[探究实验1]碱性溶液能使酚酞试液变红;
[探究实验2]碳酸盐和酸反应生成二氧化碳;
[探究实验3]鉴别碳酸钠和氢氧化钠可根据二者化学性质的不同,滴加澄清的石灰水或可溶性钙盐的溶液,根据是否生成沉淀加以区别;并根据现象推测碳酸氢钠分解的生成物,书写化学方程式;
[拓展应用]根据碳酸氢钠的性质推测其用途.
[探究实验2]碳酸盐和酸反应生成二氧化碳;
[探究实验3]鉴别碳酸钠和氢氧化钠可根据二者化学性质的不同,滴加澄清的石灰水或可溶性钙盐的溶液,根据是否生成沉淀加以区别;并根据现象推测碳酸氢钠分解的生成物,书写化学方程式;
[拓展应用]根据碳酸氢钠的性质推测其用途.
解答:解:[探究实验1]
因为碱性溶液能使酚酞变红,所以此现象说明碳酸氢钠溶液呈碱性;
[探究实验2]
碳酸氢钠和盐酸反应生成二氧化碳气体,所以会看到溶液中能产生气泡;
[探究实验3]
(1)碳酸钠能和氢氧化钙或氯化钙溶液反应生成沉淀,而氢氧化钠和氢氧化钙或氯化钙不反应,故可取少量该固体加入试管中,加适量水溶解,再滴入澄清石灰水;若观察到有白色沉淀生成,说明该白色固体是碳酸钠;
(2)碳酸氢钠受热分解生成了碳酸钠、水和二氧化碳,反应的化学方程式是2NaHCO3
Na2CO3+H2O+CO2↑;
[拓展应用]碳酸氢钠能和酸反应生成二氧化碳,故可以用作治疗胃酸的药物;受热可分解生成二氧化碳,故也可作发酵粉;
故答案为:
[探究实验1]碳酸氢钠溶液呈碱性;
[探究实验2]产生气泡;
[探究实验3](1)取少量该固体加入试管中,加适量水溶解,再滴入澄清石灰水;
(2)2NaHCO3
Na2CO3+H2O+CO2↑;
[拓展应用]治疗胃酸的药物.
因为碱性溶液能使酚酞变红,所以此现象说明碳酸氢钠溶液呈碱性;
[探究实验2]
碳酸氢钠和盐酸反应生成二氧化碳气体,所以会看到溶液中能产生气泡;
[探究实验3]
(1)碳酸钠能和氢氧化钙或氯化钙溶液反应生成沉淀,而氢氧化钠和氢氧化钙或氯化钙不反应,故可取少量该固体加入试管中,加适量水溶解,再滴入澄清石灰水;若观察到有白色沉淀生成,说明该白色固体是碳酸钠;
(2)碳酸氢钠受热分解生成了碳酸钠、水和二氧化碳,反应的化学方程式是2NaHCO3
| ||
[拓展应用]碳酸氢钠能和酸反应生成二氧化碳,故可以用作治疗胃酸的药物;受热可分解生成二氧化碳,故也可作发酵粉;
故答案为:
[探究实验1]碳酸氢钠溶液呈碱性;
[探究实验2]产生气泡;
[探究实验3](1)取少量该固体加入试管中,加适量水溶解,再滴入澄清石灰水;
(2)2NaHCO3
| ||
[拓展应用]治疗胃酸的药物.
点评:掌握碳酸盐和酸反应放出二氧化碳气体,酚酞试液的变色情况、方程式的书写,以及碳酸钠、氢氧化钠的性质,是解答的基础和关键,此外,该题还较好的考查了学生根据题意分析解决问题、应用知识解决问题的能力.

练习册系列答案
相关题目
 “中东有石油,中国有稀土”,稀土是重要的战略资源.如图是稀土元素铈在元素周期表中的相关信息,下列说法错误的是( )
“中东有石油,中国有稀土”,稀土是重要的战略资源.如图是稀土元素铈在元素周期表中的相关信息,下列说法错误的是( )| A、相对原子质量为140.1 |
| B、元素符号为Ce |
| C、铈元素属于非金属元素 |
| D、原子序数为58 |
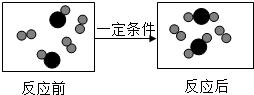 一定条件下,物质A(
一定条件下,物质A( )与B(
)与B( )反应生成C(
)反应生成C( ),下图是其反应前后分子及其数目变化的微观示意图.
),下图是其反应前后分子及其数目变化的微观示意图. 如图是某医用“葡萄糖氯化钠注射液”的部分文字说明.
如图是某医用“葡萄糖氯化钠注射液”的部分文字说明.