题目内容
15.下列生活用品中,属于有机合成材料的是( )| A. |  塑料盆 | B. |  紫砂壶 | C. |  木铲 | D. |  铁锅 |
分析 有机合成材料简称合成材料,要判断是否属于合成材料,可抓住三个特征:有机物、合成、高分子化合物,据此常见材料的分类进行分析判断.
解答 解:A、塑料盆是用塑料制成的,塑料属于三大合成材料之一,故选项正确.
B、紫砂壶是用泥土烧制而成的,属于无机非金属材料,故选项错误.
C、木铲是用木材制成的,属于天然材料,故选项错误.
D、铁锅是用生铁或钢制成的,生铁或钢属于金属材料,故选项错误.
故选:A.
点评 本题难度不大,掌握合成材料的三大特征(有机物、合成、高分子化合物)、分类是正确解答此类题的关键所在.

练习册系列答案
相关题目
5.下列叙述错误的是( )
| A. | 在牙膏中,常用轻质碳酸钙粉末作摩擦剂 | |
| B. | 日常生活中可用洗涤剂、苏打的乳化作用去除餐具上的油污 | |
| C. | 冬季使用融雪剂清雪,虽然能减少交通事故,但会对土壤造成污染 | |
| D. | 塑料回收不仅可以减少废弃塑料的数量,而且节约资源 |
6.某化学兴趣小组在实验室做了如图所示的A、B两个实验.
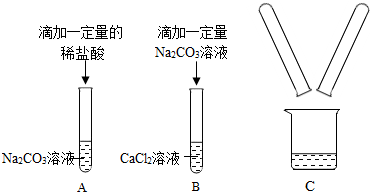
A、B两个实验结束后,小明同学将两支试管中的物质同时加入一洁净的烧杯中(如图C所示).混合后,观察到烧杯中白色沉淀明显增加,同学们将烧杯内的物质过滤,对所得滤液中溶质的成分进行探究.
【分析】A实验结束后,反应物中一定有剩余的是Na2CO3(填化学式).B实验中发生反应的化学方程式为Na2CO3+CaCl2=CaCO3↓+2NaCl.
【猜想】小明猜想:滤液中的溶质是NaCl、Na2CO3;
小滨猜想:滤液中的溶质是NaCl、CaCl2;
小英猜想:滤液中的溶质是NaCl、CaCl2、HCl;
你的猜想:滤液中的溶质是NaCl.
【讨论】你认为小英的猜想一定不合理,请说出理由若有HCl剩余,则二者溶液混合后,白色沉淀不会增加.
【实验】若要验证小明的猜想,请完成下表的方案.

A、B两个实验结束后,小明同学将两支试管中的物质同时加入一洁净的烧杯中(如图C所示).混合后,观察到烧杯中白色沉淀明显增加,同学们将烧杯内的物质过滤,对所得滤液中溶质的成分进行探究.
【分析】A实验结束后,反应物中一定有剩余的是Na2CO3(填化学式).B实验中发生反应的化学方程式为Na2CO3+CaCl2=CaCO3↓+2NaCl.
【猜想】小明猜想:滤液中的溶质是NaCl、Na2CO3;
小滨猜想:滤液中的溶质是NaCl、CaCl2;
小英猜想:滤液中的溶质是NaCl、CaCl2、HCl;
你的猜想:滤液中的溶质是NaCl.
【讨论】你认为小英的猜想一定不合理,请说出理由若有HCl剩余,则二者溶液混合后,白色沉淀不会增加.
【实验】若要验证小明的猜想,请完成下表的方案.
| 实验步骤 | 预想的实验现象 | 实验结论 |
| 取少量滤液于试管中,滴入稀盐酸 | 溶液中有气泡产生 | 小明的猜想正确 |
3.下列化学用语与意义相符的是( )
| A. | N2:表示2个氮原子 | |
| B. | Fe3O4:表示该物质中铁元素与氧元素的质量比为3:4 | |
| C. | S2-:表示硫元素显-2价 | |
| D. | C2H3OH:表示该物质由三种元素组成,且1个分子中含7个原子 |
20.下列实验方法不能达到目的是( )
| A. | 应燃烧的方法区分涤纶和羊毛 | B. | 用带火星的木条鉴别氧气和氮气 | ||
| C. | 用肥皂水将硬水转化为软水 | D. | 用氢氧化钙检验铵态氮肥 |
4.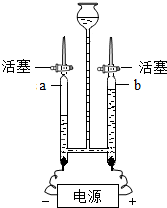 如图是电解水实验的装置图,下列说法错误的是( )
如图是电解水实验的装置图,下列说法错误的是( )
 如图是电解水实验的装置图,下列说法错误的是( )
如图是电解水实验的装置图,下列说法错误的是( )| A. | 在水中加入少量氢氧化钠以增强导电性 | |
| B. | 反应一段时间后,a、b玻璃管中产生的气体体积比约为2:1 | |
| C. | 将燃着的木条分别放在两个玻璃管尖嘴口,打开活塞,a管的气体使燃着的木条燃的更旺,b管的气体被点燃 | |
| D. | 由电解水实验得出结论:水是由氢、氧两种元素组成的 |
5.某兴趣小组的同学从超市购买一袋食盐,欲检测其是否为加碘食盐(加碘食盐中的碘元素以碘酸钾的形式存在,碘酸钾的化学式为KIO3).他们査阅资料得知,加碘食盐中的KIO3在酸性条件下能与KI溶液发生反应,生成碘(I2),淀粉遇I2变蓝色.
现提供下列试剂和生活中常见的物质:
①KI溶液②纯碱③米汤④白糖⑤白酒⑥白醋,该小组同学进行实验必须选用的试剂和物质是B.
A.①③④B.①③⑥C.②④⑥D.①④⑤
该小组经过实验确定这袋食盐是加碘食盐,同学们探究的兴趣高涨,他们仔细阅读加碘食盐包装袋上的说明后,提出问题并与其他同学讨论,继续进行实验探究.
问题一:食盐是比较稳定的,而说明中强调“防热”,是否因为受热会造成碘的损失?
【实验一】探究温度对碘损失率的影响.
老师指导他们将一定浓度的碘酸钾溶液分成5等份,在不同温度下加热十分钟后,用硫代硫酸钠标准溶液测定碘酸钾溶液的浓度,计算碘损失率并记录如表:
分析上表可得出的结论是温度越高,碘损失率越大.
问题二:炒菜时加醋对碘的损失率是否也有影响?
【实验二】探究酸碱度对碘损失率的影响.
(1)此组对照实验,要控制在碘酸钾溶液的浓度和质量、加热的时间与温度均相同,溶液的酸碱度不同的条件下进行.
(2)实验需要调节溶液的酸碱性,下列物质不能选用的是C(填字母)
A.氢氧化钠 B.纯碱粉末 C.食盐晶体 D.食醋.
现提供下列试剂和生活中常见的物质:
①KI溶液②纯碱③米汤④白糖⑤白酒⑥白醋,该小组同学进行实验必须选用的试剂和物质是B.
A.①③④B.①③⑥C.②④⑥D.①④⑤
该小组经过实验确定这袋食盐是加碘食盐,同学们探究的兴趣高涨,他们仔细阅读加碘食盐包装袋上的说明后,提出问题并与其他同学讨论,继续进行实验探究.
问题一:食盐是比较稳定的,而说明中强调“防热”,是否因为受热会造成碘的损失?
【实验一】探究温度对碘损失率的影响.
老师指导他们将一定浓度的碘酸钾溶液分成5等份,在不同温度下加热十分钟后,用硫代硫酸钠标准溶液测定碘酸钾溶液的浓度,计算碘损失率并记录如表:
| 温度 | 30℃水浴 | 50℃水浴 | 80℃水浴 | 100℃水浴 | 煮沸 |
| 碘损失率(%) | 0 | 0.3 | 0.67 | 1 | 5.56 |
问题二:炒菜时加醋对碘的损失率是否也有影响?
【实验二】探究酸碱度对碘损失率的影响.
(1)此组对照实验,要控制在碘酸钾溶液的浓度和质量、加热的时间与温度均相同,溶液的酸碱度不同的条件下进行.
(2)实验需要调节溶液的酸碱性,下列物质不能选用的是C(填字母)
A.氢氧化钠 B.纯碱粉末 C.食盐晶体 D.食醋.