题目内容
12.氧化铁(Fe2O3)和一氧化碳在高温条件下发生反应生成铁和二氧化碳,某钢铁厂购进含氧化铁85%的赤铁矿1000t,计算用这些铁矿石可炼取含杂质3%的生铁多少吨?(计算结果保留整数)分析 由赤铁矿石的质量、氧化铁的质量分数、生铁中杂质的质量分数,根据赤铁矿炼铁的化学方程式可以列式计算出理论上可以炼出含杂质3%的生铁的质量.
解答 解:设理论上可以炼出含杂质3%的生铁的质量为x.
Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2
160 112
1000t×85% (1-3%)x
$\frac{160}{1000t×85%}=\frac{112}{(1-3%)x}$
x≈613t
答:理论上可以炼出含杂质3%的生铁的质量为613t.
点评 本题难度不大,考查含杂质物质的化学方程式的计算,注意代入方程式计算的必须是纯物质的质量是正确解答此类题的关键.

练习册系列答案
 导学教程高中新课标系列答案
导学教程高中新课标系列答案
相关题目
2.如图是铱元素在元素周期表中的信息,下列说法正确的是( )


| A. | 铱原子的相对原子质量为192.2g | B. | 铱原子的核外电子数为77 | ||
| C. | 铱属于非金属元素 | D. | 铱元素符号为Ir |
20.根据你的生活经验判断,下列做法正确的是( )
| A. | 进入深洞,燃着的火把熄灭后继续前行 | |
| B. | 用清洗过的霉变大豆榨豆浆 | |
| C. | 用烧碱治疗胃酸过多 | |
| D. | 用生石灰作食品干燥剂 |
7.某实验小组用图A完成课本实验“碳酸氢钠与盐酸反应的探究”后,他们发现两种反应物的用量不同时反应后溶液中的成分也可能不同,于是他们对碳酸氢钠与盐酸反应后的大试管中溶液的成分进行探究,请回答以下问题:
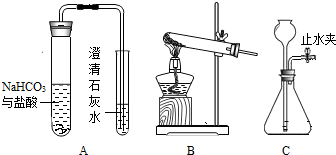
(1)写出图A中大试管发生反应的化学方程式:NaHCO3+HCl═NaCl+H2O+CO2↑;
(2)若实验室制二氧化碳应选装置C,药品为:大理石或石灰石和稀盐酸(填名称):
【提出假设】小组成员认为A中大试管的溶液的溶质只能存在三种情况:
假设1.两溶液恰好完全反应,溶质为NaCl;
假设2.两溶液完全反应后,盐酸过量,溶质为NaCl和HCl;
假设3.两溶液完全反应后,碳酸氢钠过量,溶质为NaCl和NaHCO3.
【进行实验】小组同学讨论后发现只要用反应物本身两种试剂(碳酸氢钠溶液和稀盐酸)就可以完成实验,请填写下表中的实验内容:

(1)写出图A中大试管发生反应的化学方程式:NaHCO3+HCl═NaCl+H2O+CO2↑;
(2)若实验室制二氧化碳应选装置C,药品为:大理石或石灰石和稀盐酸(填名称):
【提出假设】小组成员认为A中大试管的溶液的溶质只能存在三种情况:
假设1.两溶液恰好完全反应,溶质为NaCl;
假设2.两溶液完全反应后,盐酸过量,溶质为NaCl和HCl;
假设3.两溶液完全反应后,碳酸氢钠过量,溶质为NaCl和NaHCO3.
【进行实验】小组同学讨论后发现只要用反应物本身两种试剂(碳酸氢钠溶液和稀盐酸)就可以完成实验,请填写下表中的实验内容:
| 实验 | 实验操作 | 实验现象 | 实验结论 |
| ① | 取反应后的溶液少量于试管1中,加入过量的稀盐酸 | 有气泡产生 | 溶液中存在碳酸氢钠 假设3成立 |
| ② | 取反应后的溶液少量于试管2中,加入过量的碳酸氢钠溶液 | 有气泡产生 | 溶液中存在稀盐酸 假设2成立 |
| ③ | 综合实验①和实验②两个实验操作,发现都没有明显的实验现象 | 溶液中只存在NaCl,假设1成立 | |
2.下列关于二氧化碳性质的叙述错误的是( )
| A. | 二氧化碳能溶于水 | B. | 二氧化碳能使澄清的石灰水变浑浊 | ||
| C. | 二氧化碳用作人工降雨 | D. | 二氧化碳能与水发生反应生成碳酸 |
 下图是同学们经常使用的铅笔,在组成铅笔的各种材料中.
下图是同学们经常使用的铅笔,在组成铅笔的各种材料中.