题目内容
17.工业上,用高温煅烧石灰石的方法生产生石灰.欲生产16.8t生石灰,需含10%杂质(杂质不参加反应)的石灰石多少吨?分析 由生石灰的质量、石灰石中杂质的质量分数,根据碳酸钙高温分解的化学方程式可以列式计算出需含10%杂质(杂质不参加反应)的石灰石的质量.
解答 解:设需要这种石灰石的质量为x.
CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑
100 56
(1-10%)x 16.8t
$\frac{100}{56}=\frac{(1-10%)x}{16.8t}$ x≈33.3t
答:需要这种石灰石的质量为33.3t.
点评 本题难度不大,考查含杂质物质的化学方程式的计算,注意代入方程式计算的必须是纯物质的质量是正确解答此类题的关键.

练习册系列答案
相关题目
7.不同种元素的本质区别是( )不同.
| A. | 中子数 | B. | 质子数 | C. | 核外电子数 | D. | 相对原子质量 |
12.造成矿难的原因之一是煤层中突然有大量瓦斯逸出,其主要成分是( )
| A. | H2 | B. | CH4 | C. | CO2 | D. | CO |
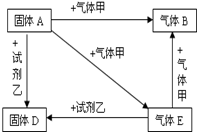 A、D是两种常见的固体,其中D为红色;B、E是两种常见的气体,其中气体E有剧毒.它们之间有如下关系:
A、D是两种常见的固体,其中D为红色;B、E是两种常见的气体,其中气体E有剧毒.它们之间有如下关系: 甲、乙、丙三种物质的溶解度曲线如图所示.
甲、乙、丙三种物质的溶解度曲线如图所示. 如图是普通白炽灯的结构.请回答下列问题.
如图是普通白炽灯的结构.请回答下列问题.