题目内容
实验时制取气体的常用装置如图所示,回答下列问题: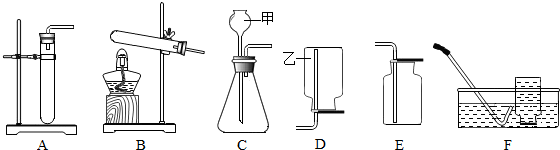
(1)写出图中仪器的名称:甲 乙
(2)利用BF组合装置制取气体
①在二氧化锰催化下,加热氯酸钾(KClO3)固体制得氧气,同时生成氯化钾,该反应的化学方程式为 ,选择B装置为气体发生装置,原因是 .利用装置F收集氧气的原因是 ;欲收集到纯净的氧气,应待到 放出时开始收集.
②利用加热高锰酸钾制取氧气时,若收集到的气体呈浅紫色,可能的错误操作是 .若该实验结束发现试管破裂了,可能的原因是 (写一点).
(3)利用CE组合装置制取气体
①制取二氧化碳的化学方程式为 .比较A和C装置,选择C装置来制备二氧化碳的优点有 (写一点).检验集满二氧化碳的方法是 .
②利用C装置制取氧气,可选用的药品为 .

(1)写出图中仪器的名称:甲
(2)利用BF组合装置制取气体
①在二氧化锰催化下,加热氯酸钾(KClO3)固体制得氧气,同时生成氯化钾,该反应的化学方程式为
②利用加热高锰酸钾制取氧气时,若收集到的气体呈浅紫色,可能的错误操作是
(3)利用CE组合装置制取气体
①制取二氧化碳的化学方程式为
②利用C装置制取氧气,可选用的药品为
考点:常用气体的发生装置和收集装置与选取方法,实验室制取氧气的反应原理,制取氧气的操作步骤和注意点,二氧化碳的实验室制法,二氧化碳的检验和验满,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:(1)由仪器的图和用途去分析;
(2)①加热氯酸钾和二氧化锰的混合物,生成氯化钾和氧气;由于反应物是固体且需要加热,由于氧气不易溶于水且不和水反应,所以可用排水法收集;用排水法收集氧气时,刚开始冒出的气泡是试管内残存的空气,只有在当气泡连续并均匀冒出时,冒出的才是氧气去分析;
②从实验室用高锰酸钾制取氧气时,要在试管口放一棉花团;实验结束时要先把导管移出水面再停止加热去分析;
(3)①从大理石(主要成分是CaCO3)和稀盐酸(主要成分HCl),二者接触即可发生反应生成氯化钙、水和二氧化碳;C装置中有长颈漏斗,可通过长颈漏斗随时加入稀盐酸;检验二氧化碳是否收集满的方法去分析;
②从C装置的特点是固体和液体反应且不需要加热去分析.
(2)①加热氯酸钾和二氧化锰的混合物,生成氯化钾和氧气;由于反应物是固体且需要加热,由于氧气不易溶于水且不和水反应,所以可用排水法收集;用排水法收集氧气时,刚开始冒出的气泡是试管内残存的空气,只有在当气泡连续并均匀冒出时,冒出的才是氧气去分析;
②从实验室用高锰酸钾制取氧气时,要在试管口放一棉花团;实验结束时要先把导管移出水面再停止加热去分析;
(3)①从大理石(主要成分是CaCO3)和稀盐酸(主要成分HCl),二者接触即可发生反应生成氯化钙、水和二氧化碳;C装置中有长颈漏斗,可通过长颈漏斗随时加入稀盐酸;检验二氧化碳是否收集满的方法去分析;
②从C装置的特点是固体和液体反应且不需要加热去分析.
解答:解:(1)由仪器的图和用途可知甲为长颈漏斗,乙为集气瓶;故答案为:长颈漏斗 集气瓶;
(2)①加热氯酸钾和二氧化锰的混合物,生成氯化钾和氧气,其化学方程式为:2KClO3
2KCl+3O2↑;由于反应物是固体且需要加热,所以发生装置应为B;由于氧气不易溶于水且不和水反应,所以可用排水法收集;用排水法收集氧气时,刚开始冒出的气泡是试管内残存的空气,只有在当气泡连续并均匀冒出时,冒出的才是氧气;
故答案为:2KClO3
2KCl+3O2↑ 反应物是固体且需要加热 氧气不易溶于水且不和水反应 气泡连续并均匀;
②实验室用高锰酸钾制取氧气时,高锰酸钾粉末会随着氧气流进入导管直到水槽,使水槽内的水变成紫红色(由于高锰酸钾溶于水显紫红色),为防止这种现象的发生,通常要在试管口放一棉花团;实验结束时要先把导管移出水面再停止加热,否则,随着试管温度的降低,试管内气体的体积越来越小,压强也越来越小,外部气压大于试管内气压,就会使水槽内的水倒吸到试管内,引起试管温度骤然降低,导致试管炸裂.故答案为:试管口没放棉花团 先停止加热再把导管拿出水面;
(3)①大理石(主要成分是CaCO3)和稀盐酸(主要成分HCl),二者接触即可发生反应生成氯化钙、水和二氧化碳.其化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;由于C装置中有长颈漏斗,可通过长颈漏斗随时加入稀盐酸;检验二氧化碳是否收集满的方法是:将燃着的木条放在集气瓶口,如果熄灭,证明已满;故答案为:CaCO3+2HCl=CaCl2+H2O+CO2↑ 随时加入稀盐酸 燃着的木条放在集气瓶口,如果熄灭,证明已满;
②由于C装置的特点是固体和液体反应且不需要加热,所以制取氧气的药品为过氧化氢溶液和二氧化锰;故答案为:过氧化氢溶液和二氧化锰.
(2)①加热氯酸钾和二氧化锰的混合物,生成氯化钾和氧气,其化学方程式为:2KClO3
| ||
| △ |
故答案为:2KClO3
| ||
| △ |
②实验室用高锰酸钾制取氧气时,高锰酸钾粉末会随着氧气流进入导管直到水槽,使水槽内的水变成紫红色(由于高锰酸钾溶于水显紫红色),为防止这种现象的发生,通常要在试管口放一棉花团;实验结束时要先把导管移出水面再停止加热,否则,随着试管温度的降低,试管内气体的体积越来越小,压强也越来越小,外部气压大于试管内气压,就会使水槽内的水倒吸到试管内,引起试管温度骤然降低,导致试管炸裂.故答案为:试管口没放棉花团 先停止加热再把导管拿出水面;
(3)①大理石(主要成分是CaCO3)和稀盐酸(主要成分HCl),二者接触即可发生反应生成氯化钙、水和二氧化碳.其化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;由于C装置中有长颈漏斗,可通过长颈漏斗随时加入稀盐酸;检验二氧化碳是否收集满的方法是:将燃着的木条放在集气瓶口,如果熄灭,证明已满;故答案为:CaCO3+2HCl=CaCl2+H2O+CO2↑ 随时加入稀盐酸 燃着的木条放在集气瓶口,如果熄灭,证明已满;
②由于C装置的特点是固体和液体反应且不需要加热,所以制取氧气的药品为过氧化氢溶液和二氧化锰;故答案为:过氧化氢溶液和二氧化锰.
点评:实验室制取气体时,发生装置的选择取决于反应物的状态和反应条件;收集装置的选择取决于水溶性和气体的密度;综合考查了实验室制取氧气和二氧化碳的反应原理,及注意事项,是考试的重点也是中考的重点.

练习册系列答案
相关题目
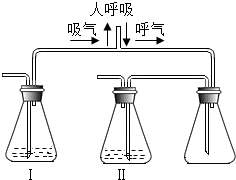 人吸入空气,排除二氧化碳等气体,为了证明人呼出的气体中含有二氧化碳且确定其中的二氧化碳不是来自于空气,某课外小组设计了如图所示的实验装置,为了除去空气中的二氧化碳气体和检验气体和检验人呼出气体中含有的二氧化碳,锥形瓶I、Ⅱ中加入的试剂为( )
人吸入空气,排除二氧化碳等气体,为了证明人呼出的气体中含有二氧化碳且确定其中的二氧化碳不是来自于空气,某课外小组设计了如图所示的实验装置,为了除去空气中的二氧化碳气体和检验气体和检验人呼出气体中含有的二氧化碳,锥形瓶I、Ⅱ中加入的试剂为( )| A、瓶I:KOH,瓶Ⅱ:NaOH |
| B、瓶INaOH,瓶Ⅱ:Ca(OH)2 |
| C、瓶I:稀盐酸,瓶Ⅱ:AgNO3 |
| D、瓶I:Na2SO4,瓶Ⅱ:BaCl2 |
下列实验操作正确的是( )
A、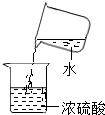 稀释浓硫酸 |
B、 点燃酒精灯 |
C、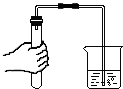 检查装置气密性 |
D、 倾倒液体药品 |
如图是甲、乙两种固体物质的溶解度曲线.下列结论正确的是( )


| A、在t2℃时,甲、乙两种物质的溶液中溶质的质量分数一定相等 |
| B、甲的溶解度大于乙的溶解度 |
| C、分别将100g甲乙两种物质的饱和溶液从t3℃降到t2℃,析出晶体的质量相等 |
| D、在t1℃时,分别在甲乙两种物质的饱和溶液中加入甲乙两种物质,所得溶液质量不变 |
下列说法正确的是( )
| A、脂肪是维持生命活动的备用能源,人应该摄入油脂 |
| B、纤维素不能被人体消化,人不应该食用富含纤维素的水果 |
| C、甲醛会破坏细菌的蛋白质结构,可用甲醛溶液来保鲜海产品 |
| D、霉变花生中的黄曲霉毒素会危害人体健康,但霉变花生煮熟后可食用 |
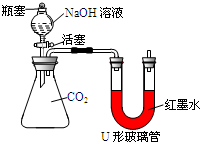 CO2通入NaOH溶液中没有明显现象,CO2与NaOH是否发生了化学反应呢?某化学兴趣小组的同学们对此进行了探究.
CO2通入NaOH溶液中没有明显现象,CO2与NaOH是否发生了化学反应呢?某化学兴趣小组的同学们对此进行了探究.