题目内容
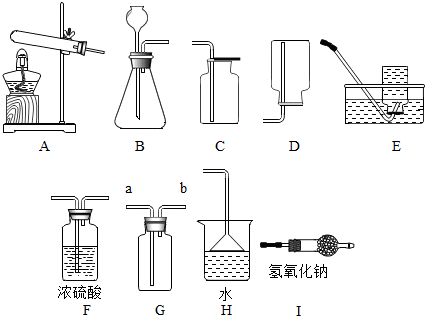
7.如图所示为实验室中常见气体制备、干燥、收集和性质实验的部分仪器(组装实验装置时,可重复选择仪器).试根据题目要求,回答下列问题: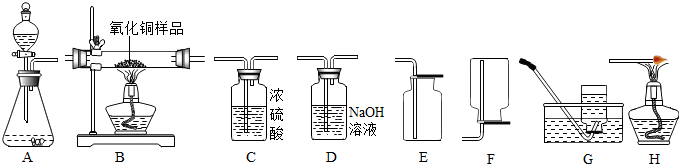
(1)小强同学以锌粒和稀硫酸为原料在实验室制备并收集一瓶纯净干燥的氢气.
①所选装置的连接顺序为A→C→F.(填写仪器序号字母).
②写出该同学制备氢气发生反应的化学方程式Zn+H2SO4=ZnSO4+H2↑.
③实验室制取氢气后的剩余废液中,可能含有少量硫酸,欲检验硫酸的存在,请你从酚酞试液、BaCl2溶液、Na2CO3溶液三种试剂中选用一种试剂进行检验,并简述选择的理由选用Na2CO3溶液,向剩余废液中加入碳酸钠溶液,若存在硫酸,就会观察到产生气泡.
(2)小静同学欲用水煤气(主要成分为一氧化碳、氢气、水蒸气等)来测定氧化铜样品中氧化铜的纯度(杂质不反应).仪器的连接顺序为 水煤气→C1→B→C2→D→H.
(已知:CuO+H2$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O,CuO+CO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2;C1、C2为2个浓硫酸的洗气瓶).
①实验时,观察到装置 B 中的现象为黑色粉末逐渐变红色.
②若装置中不连接C1,通过测定装置B反应前后的质量变化计算出样品中CuO的纯度,与实际值比较将会不受影响. (填“偏小”“偏大”“不受影响”之一)
③若实验中取用了16g氧化铜样品,反应后测定装置C1增加了0.9g,装置C2增加了1.8g,装置D增加了2.2g,则该样品中CuO的纯度为75.0%.
④若水煤气中还含有二氧化碳,仍用上述实验方案测定CuO的纯度,请谈谈你的评价意见和建议评价:反应前后装置D的增重将因水煤气混有CO2而偏大,导致计算出的CuO纯度偏大;
建议:应在气体进入装置B前,将水煤气中的CO2和水蒸气都除净,正确的实验方案设计为:
水煤气→D1→C1→B→C2→D2→H.
分析 (1)通常情况下,锌和稀硫酸反应生成硫酸锌和氢气,氢气难溶于水,密度比空气小;
浓硫酸具有吸水性,可以用来干燥氢气、氧气、二氧化碳等气体;
显酸性的溶液不能使酚酞试液变色;
稀硫酸、硫酸锌都能够和氯化钡反应生成白色沉淀硫酸钡;
碳酸钠和稀硫酸反应生成硫酸钠、水和二氧化碳;
(2)氧化铜是黑色粉末,铜是红色固体;
根据提供的数据可以计算相关方面的问题;
氢氧化钠溶液能够吸收二氧化碳气体.
解答 解:(1)①在实验室制备并收集一瓶纯净干燥的氢气,所选装置的连接顺序为A→C→F,通过A装置制取氢气,通过C装置干燥氢气,通过F装置收集氢气;
②制备氢气发生反应的化学方程式为:Zn+H2SO4=ZnSO4+H2↑;
③加入酚酞试液时,无论溶液中是否含有稀硫酸,酚酞试液都不变色,因此不能用酚酞试液检验;
加入氯化钡溶液时,无论溶液中是否含有稀硫酸,都产生白色沉淀,因此不能用氯化钡溶液检验;
加入碳酸钠溶液时,如果有稀硫酸,则产生气泡,如果无稀硫酸,则不产生气泡,因此可以用碳酸钠溶液检验.
故填:A→C→F;Zn+H2SO4=ZnSO4+H2↑;选用Na2CO3溶液,向剩余废液中加入碳酸钠溶液,若存在硫酸,就会观察到产生气泡.
(2)①实验时,观察到装置B中的现象为黑色粉末逐渐变红色;
②若装置中不连接C1,通过测定装置B反应前后的质量变化计算出样品中CuO的纯度,因为水蒸气不影响对装置B反应前后的质量变化的计算,因此与实际值比较将不受影响;
③设与氢气反应的氧化铜质量为x,与一氧化碳反应的氧化铜质量为y,
反应后测定装置C2增加了1.8g,说明生成了1.8g水,装置D增加了2.2g,说明生成了2.2g二氧化碳,
CuO+H2$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O,CuO+CO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2,
80 18 80 44
x 1.8g y 2.2g
$\frac{80}{x}$=$\frac{18}{1.8g}$,$\frac{80}{y}$=$\frac{44}{2.2g}$,
x=8.0g,y=4.0g,
则该样品中CuO的纯度为:$\frac{8.0g+4.0g}{16g}$×100%=75.0%;
④评价:反应前后装置D的增重将因水煤气混有CO2而偏大,导致计算出的CuO纯度偏大;
建议:应在气体进入装置B前,将水煤气中的CO2和水蒸气都除净,正确的实验方案设计为:
水煤气→D1→C1→B→C2→D2→H.
故填:黑色粉末逐渐变红色;不受影响;75.0%;
评价:反应前后装置D的增重将因水煤气混有CO2而偏大,导致计算出的CuO纯度偏大;
建议:应在气体进入装置B前,将水煤气中的CO2和水蒸气都除净,正确的实验方案设计为:水煤气→D1→C1→B→C2→D2→H.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

| A. |  | B. |  | C. |  | D. |  |
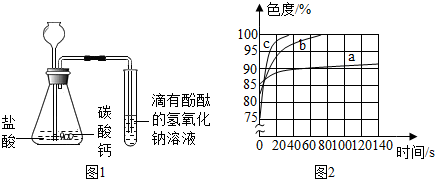
【提出问题】是什么原因导致滴有酚酞的NaOH溶液由红色褪为无色?
【猜想与假设】他们分别对这种意外现象作如下猜想:
甲同学:可能是酚酞与O2发生了反应;
乙同学:可能是NaOH溶液与空气中的CO2发生了反应;
丙同学:可能与氢氧化钠溶液的浓度大小有关;
【设计实验】三位同学分别设计实验验证自己的猜想:
(1)甲同学设计了如下实验,请你填写下表.
| 实验步骤 | 设计这一步骤的目的 | 实验现象 | 实验结论 |
| ①将NaOH溶液加热煮沸 | ①除去溶液中的氧气 | 溶液变红,过一会儿红色消失 | 甲同学猜想不正确(填“正确”或不正确”) |
| ②向冷却后的溶液中滴人酚酞,并滴一些植物油在其上方 | ②隔绝氧气 |
(3)丙同学使用了色度传感器测溶液的颜色.他在a、b、c三个比色皿中分别加入等量5%、10%、20%
的NaOH溶液,然后各滴加2滴酚酞试液.溶液颜色的变化曲线如图[说明:溶液无色 时色度值(透过率)为100%].请你观察图二写出规律性结论:氢氧化钠溶液的浓度越大,酚酞试液变红后褪色越快;氢氧化钠溶液的浓度越小,色度值越大..
| A. | Ba2+、Cu2+、SO42- | B. | Na+、OH-、Cl- | C. | K+、Cl-、MnO4- | D. | H+、Ca2+、CO32- |
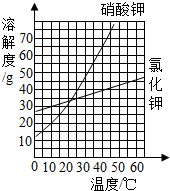 如图是氯化钾和硝酸钾两种固体溶解度曲线图.
如图是氯化钾和硝酸钾两种固体溶解度曲线图. 请回答以下问题.
请回答以下问题.