题目内容
11. 构建知识网络是学习化学的重要方法,如图是不同物质相互转化关系图.其中A、B、C、D属于不同类别的物质,且都含有铜元素,B为黑色粉末,C为红色粉末.“→”表示一种物质一步转化成另一种物质(部分反应物、生成物及反应条件未标出),请回答问题:
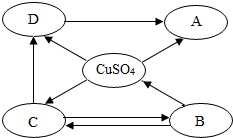
构建知识网络是学习化学的重要方法,如图是不同物质相互转化关系图.其中A、B、C、D属于不同类别的物质,且都含有铜元素,B为黑色粉末,C为红色粉末.“→”表示一种物质一步转化成另一种物质(部分反应物、生成物及反应条件未标出),请回答问题:(1)C的化学式Cu,A的化学式Cu(OH)2.
(2)写出由B生成硫酸铜的化学方程式CuO+H2SO4=CuSO4+H2O.
(3)由CuSO4生成C的反应的微观实质是Fe+Cu2+═Fe2++Cu.
分析 A、B、C、D属于不同类别的物质,且都含有铜元素,B为黑色粉末,因此B是氧化铜,C为红色粉末,因此C为铜;C-铜能够转化为D,应该是铜和硝酸银等盐溶液反应产生铜盐,如硝酸铜;铜盐和硫酸铜都能够转化为不同类别的A,因此A是氢氧化铜,带入验证符合转化关系完成相关的问题.
解答 解:A、B、C、D属于不同类别的物质,且都含有铜元素,B为黑色粉末,因此B是氧化铜,C为红色粉末,因此C为铜;C-铜能够转化为D,应该是铜和硝酸银等盐溶液反应产生铜盐,如硝酸铜;铜盐和硫酸铜都能够转化为不同类别的A,因此A是氢氧化铜,因此:
(1)C是铜,A是氢氧化铜,故填:Cu;Cu(OH)2;
(2)由氧化铜和硫酸反应可以生成硫酸铜,故反应的方程式为:CuO+H2SO4=CuSO4+H2O;
(3)由CuSO4生成Cu的反应可以是铁和硫酸铜反应产生的硫酸亚铁和铜,反应的方程式为:Fe+CuSO4═FeSO4+Cu,反应的微观实质是铁和铜离子结合产生亚铁离子和铜;故答案为:Fe+Cu2+═Fe2++Cu.
点评 本题为框图型物质推断题,完成此类题目,可以依据题干提供的信息,结合框图,找准解题的突破口,直接得出物质的化学式,然后顺推或逆推或由两边向中间推得出其他物质的化学式.

练习册系列答案
相关题目
3.已知:在一定条件下,同一化学反应进行的快慢与反应物的质量分数成正比,产生H2的总质量与溶液中H+的总质量有关.现用100g3%的硫酸溶液与过量的锌粉反应,为了使反应慢点而又不影响生成氢气的总质量,可向所用的硫酸溶液中加入适量的( )
①氢氧化钠②水③硫酸钠稀溶液④氯化钡稀溶液⑤碳酸钠溶液.
①氢氧化钠②水③硫酸钠稀溶液④氯化钡稀溶液⑤碳酸钠溶液.
| A. | ②③ | B. | ②③④ | C. | ③④⑤ | D. | ①④⑤ |
15.香蕉等水果具有芳香气味,是因为其中含有乙酸乙酯( C4H8O2)等物质.下列关于乙酸乙酯的说法不正确的是( )
| A. | 每个分子由4个碳原子、8个氢原子和2个氧原子构成 | |
| B. | 属于氧化物 | |
| C. | 碳、氢、氧三种元素质量比为6:1:4 | |
| D. | 相对分子质量为88 |
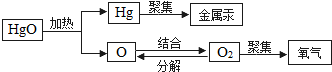 化学是在原子、分子水平上研究物质及其变化的科学.
化学是在原子、分子水平上研究物质及其变化的科学.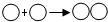 表示氧分子的形成过程
表示氧分子的形成过程