题目内容
以下是初中化学的一些基本实验:
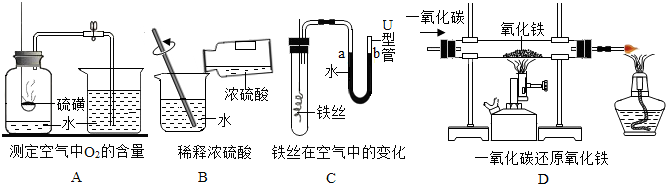
(1)上述实验中不能达到实验目的是 (填字母).
(2)A中可燃物应取过量的原因是 ;B中玻璃棒的主要作用是 .过一段时间后C中的实验现象为 .
(3)D中硬质玻璃管内发生反应的化学方程式为 .

(1)上述实验中不能达到实验目的是
(2)A中可燃物应取过量的原因是
(3)D中硬质玻璃管内发生反应的化学方程式为
考点:空气组成的测定,浓硫酸的性质及浓硫酸的稀释,一氧化碳还原氧化铁,金属锈蚀的条件及其防护,书写化学方程式、文字表达式、电离方程式
专题:实验性简答题
分析:(1)A、B、C、D四个实验中:A实验生成物为二氧化碳气体,不能形成气压差,故不能达到实验目的;而B、C、D三个实验可以完成,能够能达到实验目的;
(2)①A实验测定空气中氧气的含量,故应充分消耗氧气;
②B实验稀释浓硫酸,玻璃棒搅拌并及时散热;
③C实验铁丝生锈消耗空气中的氧气,管内外形成气压差,故U型管中液面左高右低;
④D实验一氧化碳还原氧化铁,已知反应物一氧化碳和氧化铁,生成物为二氧化碳和铁,反应条件为高温;反应完,将有尾气一氧化碳,故需要处理掉.
(2)①A实验测定空气中氧气的含量,故应充分消耗氧气;
②B实验稀释浓硫酸,玻璃棒搅拌并及时散热;
③C实验铁丝生锈消耗空气中的氧气,管内外形成气压差,故U型管中液面左高右低;
④D实验一氧化碳还原氧化铁,已知反应物一氧化碳和氧化铁,生成物为二氧化碳和铁,反应条件为高温;反应完,将有尾气一氧化碳,故需要处理掉.
解答:解:
(1)经分析A、B、C、D四个实验,A实验生成物为二氧化碳气体,不能形成气压差,故不能达到实验目的;
(2)
①A中可燃物应取过量的原因是确保集气瓶中的氧气完全反应;
②B中玻璃棒的作用是搅拌、散热;
③一段时间后,C中的实验现象为铁丝生锈,U型管中液面左高右低;
④D中硬质玻璃管内发生反应的化学方程式为Fe2O3+3CO
2Fe+3CO2.
故答案为:
(1)A;
(2)确保集气瓶中的氧气完全反应;搅拌、散热;铁丝生锈,U型管中液面左高右低;
Fe2O3+3CO
2Fe+3CO2.
(1)经分析A、B、C、D四个实验,A实验生成物为二氧化碳气体,不能形成气压差,故不能达到实验目的;
(2)
①A中可燃物应取过量的原因是确保集气瓶中的氧气完全反应;
②B中玻璃棒的作用是搅拌、散热;
③一段时间后,C中的实验现象为铁丝生锈,U型管中液面左高右低;
④D中硬质玻璃管内发生反应的化学方程式为Fe2O3+3CO
| ||
故答案为:
(1)A;
(2)确保集气瓶中的氧气完全反应;搅拌、散热;铁丝生锈,U型管中液面左高右低;
Fe2O3+3CO
| ||
点评:了解金属生锈的条件,探究测定空气中氧气含量的方法;掌握浓硫酸的性质和稀释方法及其注意事项;掌握一氧化碳还原氧化铁的实验原理及注意事项.

练习册系列答案
 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
下列关于溶液的说法中,正确的是( )
| A、泥水中,泥是溶质,水是溶剂 |
| B、物质的溶解过程通常会伴随着能量的变化 |
| C、配制溶液时,搅拌可以增大固体物质的溶解度 |
| D、饱和溶液就是不能再溶解任何物质的溶液 |
实验室制氧气不需要用到的仪器是( )
| A、酒精灯 | B、集气瓶 |
| C、胶塞 | D、烧杯 |
下列有关实验操作的叙述,正确的是( )
| A、取用液体药品,如果未说明用量,一般用10-20ml |
| B、烧杯和蒸发皿都可以直接在酒精灯外焰上加热 |
| C、过滤器中滤纸边缘应低于漏斗边缘 |
| D、取用固体粉未可用药匙或镊子 |