题目内容
4.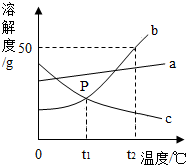 根据如图中a、b、c三种物质的溶解度曲线,回答下列问题:
根据如图中a、b、c三种物质的溶解度曲线,回答下列问题:(1)P点的含义是t1℃时b和c的溶解度相等
(2)t2℃,a、b、c三种物质的饱和溶液溶质质量分数的大小关系为b>a>c.
(3)t2℃时,50g b物质加入到50g水中充分溶解后,所得溶液的质量为75g.
(4)b中含有少量的a,若要提纯b,可采用降温结晶的方法.
分析 (1)P点是bc两物质溶解度曲线的交点,表示在该温度下,两物质的溶解度相同;
(2)根据溶解度曲线解答;
(3)根据b物质在t2℃时的溶解度解答;
(4)b物质的溶解度随温度的升高而升高.a的溶解度受温度影响不大.
解答 解:(1)曲线中交点表示该温度时两种物质的溶解度相等,所以t1℃温度时,b和c物质的溶解度相等;
(2)根据溶解度曲线,t2℃时,a、b、c三种物质的溶解度是b>a>c,故三种物质的饱和溶液溶质质量分数的大小关系为b>a>c;
(3)t2℃时,b物质溶解度是50g,100g水中溶解50g,50g水中最多溶解25g,故所得溶液的质量为75g;
(4)b物质的溶解度随温度的升高而升高.a的溶解度受温度影响不大,b中含有少量的a,若要提纯b,可采用冷却热饱和溶液法,故答案为:冷却热饱和溶液法.
故答案为:(1)t1℃时,b和c物质的溶解度相等;(2)b>a>c;(3)75g;(4)降低.
点评 根据溶解度曲线,判断某种物质在不同温度下的溶解度的大小;比较不同物质在同一温度时溶解度的大小;判断物质的溶解度受温度影响变化的趋势等.

练习册系列答案
相关题目
14.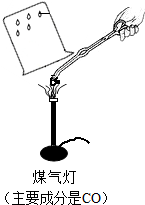 石灰石是常用的建筑材料.
石灰石是常用的建筑材料.
甲乙同学设计了如下实验方案进行探究:
Ⅰ.甲同学取石灰石按图所示进行实验(煤气灯能达到石灰石分解的温度),
观察到烧杯内壁石灰水变浑浊,由此甲同学认为石灰石已分解.
甲同学结论不合理的理由是煤气灯的燃料的主要成分为一氧化碳,而一氧化碳燃烧生成了二氧化碳,所以澄清石灰水变浑浊不一定是来源于石灰石的分解.
写出石灰水变浑浊的化学方程式Ca(OH)2+CO2=CaCO3↓+H2O.
Ⅱ.乙同学进行如下实验,完成下表:
Ⅲ.为了测定某石灰石中碳酸钙的质量分数(假设杂质不参加反应,且不溶于水),某兴趣小组设计如下实验方案:①称取10g石灰石样品,②高温煅烧至质量不再改变,③把剩余固体放在空气中冷却至室温,④称得剩余固体的质量为6.04g.(相对原子质量:Ca-40 O-16 C-12)
①根据方案计算石灰石中碳酸钙的质量分数(根据化学方程式列式计算).
②指出该实验方案中一处明显的不足并说明原因氧化钙会吸收空气中的水分.
 石灰石是常用的建筑材料.
石灰石是常用的建筑材料.甲乙同学设计了如下实验方案进行探究:
Ⅰ.甲同学取石灰石按图所示进行实验(煤气灯能达到石灰石分解的温度),
观察到烧杯内壁石灰水变浑浊,由此甲同学认为石灰石已分解.
甲同学结论不合理的理由是煤气灯的燃料的主要成分为一氧化碳,而一氧化碳燃烧生成了二氧化碳,所以澄清石灰水变浑浊不一定是来源于石灰石的分解.
写出石灰水变浑浊的化学方程式Ca(OH)2+CO2=CaCO3↓+H2O.
Ⅱ.乙同学进行如下实验,完成下表:
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量煅烧后固体于试管中,加水振荡,过滤,取滤液,滴加酚酞溶液 | 溶液变红 | 证明固体中含有氧化钙 |
| 取滤渣滴加足量的稀盐酸 | 有气泡产生 | 含有碳酸钙 |
①根据方案计算石灰石中碳酸钙的质量分数(根据化学方程式列式计算).
②指出该实验方案中一处明显的不足并说明原因氧化钙会吸收空气中的水分.
15.2016年4月22日是第47个世界地球日,下列做法中错误的是( )
| A. | 回收废旧电池,既可节约金属资源又可减少环境污染 | |
| B. | 推广无纸化办公,使用再生纸且双面打印 | |
| C. | “低碳生活”倡导、鼓励人们多开汽车出行 | |
| D. | 使用可降解塑料代替传统塑料,有利于减轻“白色污染” |
19.下列实验操作错误的是( )
| A. | 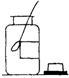 | B. | 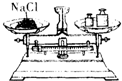 | C. |  | D. | 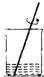 |
9.下列是有关实验操作的步骤和做法,正确的是( )
| A. | 粗盐提纯操作的顺序是:溶解、过滤、蒸发、洗涤 | |
| B. | 实验室制取氧气完毕后,应先停止加热,再取出导管 | |
| C. | 不慎将浓硫酸洒在桌上,应先用烧碱溶液中和,再用湿布抹净 | |
| D. | 用试管夹夹持试管时,把试管夹从试管底部往上套,夹在试管中上部 |
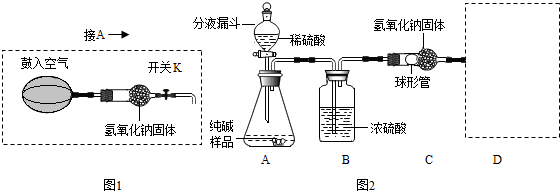
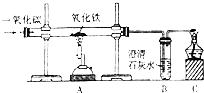 在实验室里,可以利用如图装置制得铁,请回答下列问题:
在实验室里,可以利用如图装置制得铁,请回答下列问题: