题目内容
15.如图所示为实验室常用的实验装置: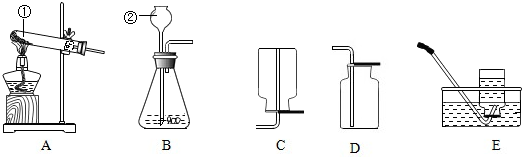
据此回答下列问题:
(1)写出标号所示仪器的名称:①试管,②长颈漏斗.
(2)常温下,用大理石和稀盐酸反应制取二氧化碳,应选用的发生装置是B(填序号,下同),收集装置是D.
(3)实验室通常用加热高锰酸钾固体的方法制取氧气,该反应的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,应选用的发生装置是
A,收集装置是D或E;此外,也可以用分解过氧化氢(H2O2)的方法制取氧气,该反应的化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,用这种方法制取氧气,应选用的发生装置是B.
分析 (1)要熟悉各种仪器的名称、用途和使用方法;
(2)实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,反应不需要加热,大理石和石灰石的主要成分是碳酸钙,能和稀盐酸反应生成氯化钙、水和二氧化碳; 二氧化碳能够溶于水,密度比空气大;
(3)高锰酸钾受热时能够分解生成锰酸钾、二氧化锰和氧气;
氧气的密度比空气的密度大,不易溶于水;通常情况下,过氧化氢在二氧化锰的催化作用下,分解生成水和氧气来分析.
解答 解:(1)①是试管;②是长颈漏斗.
故填:试管;长颈漏斗.
(2)用大理石和稀盐酸反应制取二氧化碳不需要加热,应选用的发生装置是B装置;
二氧化碳能够溶于水,不能用排水法收集,密度比空气大,可以用向上排空气法收集,即用D装置收集;
故填:B;D;
(3)在实验室用高锰酸钾的方法来制取氧气需要加热,应选用的发生装置是A装置;
因为氧气的密度比空气大,可以用向上排空气法收集,即用D装置收集,氧气不易溶于水,可以用排水法收集,即用E装置收集;
反应的化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
常温下,在过氧化氢(H2O2)溶液中加入MnO2(固体粉末)即可制取氧气.用这种方法制取氧气时,过氧化氢以二氧化锰为催化剂生成水和氧气,反应物的状态是固态和液态,反应条件是常温,应选固-液不加热型的发生装置,应选用的发生装置是B;
故填:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;A;D或E;2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;B.
点评 本题主要考查仪器的用途、反应表达式的书写,实验装置的选择,选择发生装置时,要考虑反应物的状态、反应条件等因素;选择收集装置时,要考虑气体的水溶性、能否和水发生化学反应、密度、能否和空气中的物质发生化学反应等因素.

 轻松暑假总复习系列答案
轻松暑假总复习系列答案
| A. | 原子序数是16 | B. | 它是金属元素 | ||
| C. | 核内质子数是32 | D. | 相对原子质量是16 |
| A. | 二氧化碳不支持燃烧,通常可用于灭火 | |
| B. | 盐酸可与金属氧化物反应,可用于金属除锈 | |
| C. | 氢氧化钠可与酸发生中和反应,可用于治疗胃酸过多 | |
| D. | 氧气具有氧化性,可用于抢救危重病人 |
| A. | 二氧化碳 | B. | 铁 | C. | 水 | D. | 氯化钠 |
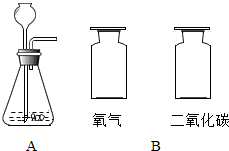 某校的兴趣小组的同学对目前市面上买的“发热贴”进行探究.通过实验探究发热贴是否真的只能与氧气反应发热,在缺氧的环境下(只有二氧化碳的环境)不能放热.
某校的兴趣小组的同学对目前市面上买的“发热贴”进行探究.通过实验探究发热贴是否真的只能与氧气反应发热,在缺氧的环境下(只有二氧化碳的环境)不能放热.