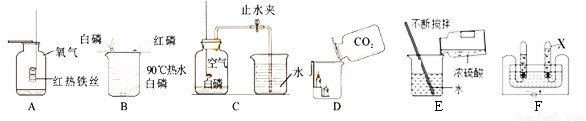
��Ŀ����
����ش����ϣ�ˮ��Դ�����Ϸḻ�������й�ˮ��˵����ȷ����
A. ��Ȼ���ˮ��Ӳˮ���ڻ�����ˮ���ڴ�����
B. ˮ����ԭ�Ӻ���ԭ�ӹ���
C. ˮ�м���һ���������ǿ���������ǿ�䵼����
D. ����ˮ���������м�������������������ˮ�������������ٽ������
D ��������A��Ӳˮ����ˮ���ǻ���ֻ��Ӳˮ�к��н϶�Ŀ����Եĸ�þ���������ˮ�к��н��ٵĿ����Ը�þ������ʴ��� B��ˮ����ˮ���ӹ��ɵģ����� C���������ɷ��ӹ��ɣ����Ӳ��Ե��ԣ�������ˮ�к����Բ���������ǿ������ D������ˮ���������м�������������������ˮ�������������ٽ����������ȷ����ѡD��
��ϰ��ϵ�д�
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
�����Ŀ
��ȥ���������е��������ʣ���ѡ�Լ����������ȽϺ�������
ѡ�� | ���� | ���� | �Լ��Ͳ������� |
A | �Ȼ��� | ̼���� | �ӹ�����ϡ���ᣬ�����ᾧ |
B | ���� | ˮ | ���������ͨ��Ũ���� |
C | �Ȼ��� | �Ȼ�þ | ������������������Һ�����ˡ�ϴ�ӡ����� |
D | ����ͭ | ���� | ������ͭ�� |
A. A B. B C. C D. D
A ��������A��̼�������������ϡ���ᷴӦ�����Ȼ��ơ�ˮ�Ͷ�����̼�����������ᾧ���ܳ�ȥ������û�������µ����ʣ����ϳ���ԭ����ȷ��B��Ũ���������ˮ�ԣ������뵪����Ӧ�������ܰ����ʳ�ȥ��Ҳ���ԭ���ʳ�ȥ�������ϳ���ԭ����C���Ȼ�þ������������������Һ��Ӧ����������þ�������Ȼ��أ����˼��ɳ�ȥ����������Ҫϴ�Ӻ�������ϳ���ԭ����D��ͭ��������ͭ�����ᶼ����Ӧ�����ܳ��ӣ�����...ij����Ƭ����ˮʱ����ɷ���̼������(NaHCO3)��������(C6H8O7����Է�������Ϊ192)������Ӧ��ԭ��Ϊ��3NaHCO3 + C6H8O7 = Na3C6H5O7 + 3H2O + 3CO2������1Ƭ����Ƭ(4 g/Ƭ)����ʢ������ˮ���ձ��У���¼�ձ��������������仯�����ʾ��(��������ȫ����ɢ����Ӧ��ǡ����ȫ��Ӧ)
��Ӧʱ��/min | 0 | t1 | t2 | t3 | t4 |
������/g | 250.00 | 249.68 | 249.48 | 249.34 | 249.34 |
���ݻ�ѧ����ʽ���㣺ÿƬ����Ƭ�����������������Ϊ______________��
24% �����������ݷ�Ӧ�Ļ�ѧ����ʽ�����𡣷�Ӧ���ɶ�����̼������= 250.00g-249.34g=0.66g����ÿƬ����Ƭ�����������������Ϊx�� 3NaHCO3 + C6H8O7 = Na3C6H5O7 + 3H2O + 3CO2�� 192 132 x 0.66g x=0.96g ÿƬ����Ƭ�����������������Ϊ��100��=24�� ��ÿƬ����Ƭ����...