题目内容
19.市场上有两种外观类似黄金的Cu•Zn合金和Cu•Ag合金制品,若实验室只提供一瓶稀硫酸和必要仪器.(1)你认为能测出Cu-Zn合金中铜的质量分数;
(2)取上述(1)中的合金粉末20g放入烧杯中,加入50g的稀硫酸,恰好完全反应,测得烧杯内剩余物的质量为69.8g.求:该合金中铜的质量分数.
分析 (1)因为Zn的金属活动性在(H)之前,可与稀硫酸发生置换反应,而Cu和Ag的金属活动性在(H)之后,不能与稀硫酸发生置换反应;
(2)根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和.所以生成氢气的质量=参加反应前各物质的质量总和-反应后生成各物质的质量总和;
根据锌与稀硫酸反应的化学方程式和生成氢气的质量,列出比例式,就可计算出该合金中锌的质量,该合金中铜的质量=合金质量-该合金中锌的质量,然后根据“$\frac{合金中铜的质量}{合金质量}$×100%”计算即可;
解答 解:(1)Cu-Ag合金中的Cu和Ag都不能与稀硫酸发生置换反应,Cu-Zn合金中的Zn可与稀硫酸发生置换反应,故能测出Cu-Zn合金中铜的质量分数.故答案为:Cu-Zn;
(2)产生氢气的质量=20g+50g-69.8g=0.2g;
设该合金中锌的质量为x;
则:产生氢气的质量为:50g+20g-69.8g=0.2g
Zn+H2SO 4=ZnSO4+H2↑
65 2
X 0.2g
∴65:2=X:0.2g
∴x=6.5g
则该合金中铜的质量分数为:(20g-6.5g)÷20g×100%=67.5%;
答:该合金中铜的质量分数为67.5%;
点评 本题主要考查学生对金属的化学性质的认识,以及运用化学方程式和溶质质量分数公式综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
相关题目
10.下列物质在应用时,用到其物理性质的是( )
| A. |  在食品袋内充氮气防腐 | B. |  用明矾净水 | ||
| C. |  用稀有气体制闪光灯 | D. |  用二氧化碳作气体肥料 |
7.甲、乙两种物质的溶解度曲线如图所示,下列有关叙述正确的是( )
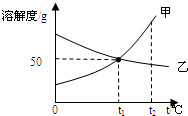

| A. | t1℃时,甲、乙溶液的溶质质量分数相等 | |
| B. | t1℃时,甲的饱和溶液中含50g溶质 | |
| C. | t1℃时,甲的饱和溶液升高温度后溶解度变大,溶质质量分数不变 | |
| D. | 甲物质的溶解度大于乙物质的溶解度 |
14.如表是某同学用多种方法来鉴别物质的情况,其中完全正确的是( )
| 需鉴别物质 | 分别取样后所加试剂或方法 | ||
| 方法1 | 方法2 | ||
| A | 硝酸铵和氢氧化钠 | 加适量水看是否溶解 | 加熟石灰研磨并闻气味 |
| B | 鉴别厕所清洁剂(含盐酸)和洗衣液 | 加入酚酞溶液,观察现象 | 加入小苏打,观察现象 |
| C | 木炭粉末和氧化铜粉末 | 稀硫酸 | 加水溶解 |
| D | 黄铜和黄金 | 互相刻划,比较硬度 | 观察颜色 |
| A. | A | B. | B | C. | C | D. | D |
4.某反应的微观示意图如下,下列说法不正确的是( )
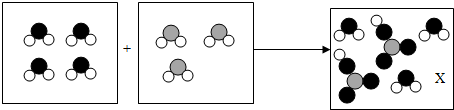

| A. | 两种反应物的分子数目之比为4:3 | B. | X是 | ||
| C. | 该反应中分子的数目发生了变化 | D. | 该反应中原子的种类不变 |
11.下列有关叙述中,不正确的是( )
| A. | H2、C和CO都有还原性,可用于冶炼金属 | |
| B. | 物质的热胀冷缩现象说明分子原子间存在间隔 | |
| C. | 稀盐酸和食醋都能使紫色石蕊溶液变红 | |
| D. | 我们使用的2B铅笔的制作材料是有机物和和铅 |
8.“吸烟有害健康”,香烟的烟气中含有上百种有毒物质,其中一种物质极易与血红蛋白结合.该物质是( )
| A. | SO2 | B. | CO | C. | CO2 | D. | NO2 |
2.某化学反应的微观示意图为: (
( 、
、 代表不同原子),关于该反应的说法正确的是( )
代表不同原子),关于该反应的说法正确的是( )
 (
( 、
、 代表不同原子),关于该反应的说法正确的是( )
代表不同原子),关于该反应的说法正确的是( )| A. | 涉及到五种物质 | B. | 分子的种类不变 | C. | 属于分解反应 | D. | 原子的种类不变 |