题目内容
5.只含铜和氧两种元素的固体样品9.0g,测得铜的质量为8.0g.已知铜的氧化物有CuO和Cu2O,下列说法正确的是( )| A. | 固体样品可能是Cu2O | |
| B. | 固体样品一定是CuO与Cu2O的混合物 | |
| C. | 固体样品的组成只有两种情况 | |
| D. | 若固体样品由两种物质组成,则其中一种质量分数为$\frac{4}{9}$ |
分析 根据题目可知,固体样品中铜元素和氧元素的质量分别为8g和1g,那么固体样品中铜原子和氧原子的个数比为2:1.所以固体样品可能为Cu2O,也可能是Cu、CuO,也可能是Cu、CuO与Cu2O,但不可能是CuO与Cu2O两种物质组成的混合物.
解答 解:这道题目只要是给定元素的质量,推测物质的组成,关键在于寻找元素的质量与原子个数之间的关系.$\frac{元素的质量}{相对原子的质量}$与原子个数之间存在等比例关系.
由题意可知,铜元素质量为8g,则固体样品中氧元素质量为1g,则铜、氧原子个数比为 $\frac{8g}{64}$:$\frac{1g}{16}$=2:1,即固体样品中铜、氧元素的平均组成为Cu2O.可能为纯净物Cu2O,也可能是Cu和CuO或Cu、Cu2O、CuO,但不可能是CuO与Cu2O两种物质组成的混合物.
对于D选项:如果固体样品是由两种物质组成,则为Cu和CuO的组合.设固体样品中Cu的质量为x,则CuO的质量为(9g-x),由题意,x+(9g-x)×$\frac{64}{80}$=8g,x=4g,即Cu在固体样品中的质量分数为$\frac{4}{9}$.
A、固体样品可能是Cu2O,故正确;
B、固体样品一定是CuO与Cu2O的混合物,说法错误,因为由铜、氧原子个数比为 2:1,则“不可能是CuO与Cu2O两种物质组成的混合物”,故错误;
C、固体样品的组成只有2种情况,说法错误,因为“可能为纯净物Cu2O,也可能是Cu和CuO或Cu、Cu2O、CuO”,故错误;
D、若固体样品由两种物质组成,则为Cu和CuO的组合,而Cu在固体样品中的质量分数为$\frac{4}{9}$,故D正确.
故选AD.
点评 这类试题要求学生有较强的数据分析能力和数据处理能力,从而培养了各科间的融合能力.

| A. | 散热的速度加快 | B. | 提高空气中氧气的含量 | ||
| C. | 降低木材的着火点 | D. | 增大木材与空气的接触面积 |
| A. | 臭氧是一种单质 | B. | 臭氧是氧气 | ||
| C. | 臭氧由3个氧原子构成 | D. | 臭氧中氧元素的化合价为-2价 |

 请回答下列问题.
请回答下列问题.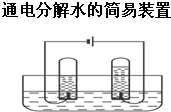 根据电解水的实验装置图完成下列问题:
根据电解水的实验装置图完成下列问题: