题目内容
19.向含有稀硫酸和硫酸铜的混合溶液中滴加NaOH溶液,如图曲线中描述正确的是( )| A. | 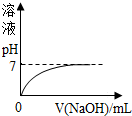 | B. | 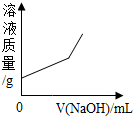 | C. | 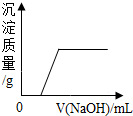 | D. | 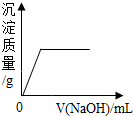 |
分析 A、根据稀硫酸和硫酸铜的混合溶液的pH值不可能为零进行分析;
B、根据氢氧化钠和硫酸反应生成硫酸钠和水,氢氧化钠和硫酸铜反应生成氢氧化铜沉淀和硫酸钠进行分析;
C、根据向含有稀硫酸和硫酸铜的混合溶液中滴加NaOH溶液,氢氧化钠会先于硫酸反应,再与硫酸铜反应进行分析;
D、根据向含有稀硫酸和硫酸铜的混合溶液中滴加NaOH溶液,氢氧化钠会先于硫酸反应,再与硫酸铜反应进行分析.
解答 解:A、硫酸和硫酸铜的混合溶液的pH值不可能为零,所以曲线可能从零开始,故A错误;
B、氢氧化钠和硫酸反应生成硫酸钠和水,氢氧化钠和硫酸铜反应生成氢氧化铜沉淀和硫酸钠,刚开始溶液质量增大,生成的氢氧化铜的质量大于参加反应的氢氧化钠的质量,所以一段时间后,溶液质量减少,故B错误;
C、向含有稀硫酸和硫酸铜的混合溶液中滴加NaOH溶液,氢氧化钠会先于硫酸反应,再与硫酸铜反应,所以加入一定量的氢氧化钠后才会出沉淀,故C正确;
D、向含有稀硫酸和硫酸铜的混合溶液中滴加NaOH溶液,氢氧化钠会先于硫酸反应,再与硫酸铜反应,所以加入一定量的氢氧化钠后才会出沉淀,故D错误.
故选:C.
点评 本题是化学反应与图象知识的考查题,结合反应的过程与图象情况的走势联系起来是解题的关键所在.

练习册系列答案
相关题目
11.下列对分子、原子、离子的认识正确的是( )
| A. | 原子是最小的粒子,不可再分 | B. | 钠原子失去1个电子形成Na- | ||
| C. | 离子不能直接构成物质 | D. | 原子质量主要集中在原子核上 |
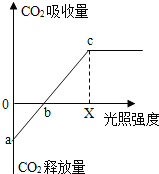 植物的光合作用和呼吸作用强度可以用单位时间内吸收或释放二氧化碳的量来表示.曲线表示在恒温30℃时,某植物在不同光照强度下,吸收二氧化碳与释放二氧化碳量的关系,试回答下列问题:
植物的光合作用和呼吸作用强度可以用单位时间内吸收或释放二氧化碳的量来表示.曲线表示在恒温30℃时,某植物在不同光照强度下,吸收二氧化碳与释放二氧化碳量的关系,试回答下列问题: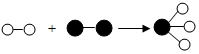 德国化学家格哈德•埃特尔,因在“固体表面的化学反应”研究中取得了开拓性成就而获得诺贝尔化学奖.他的成就之一是证实了氢气与氮气在固体催化剂表面合成氨气的反应过程.如图所示是该反应的模型图 (○表示氢原子,●表示氮原子)
德国化学家格哈德•埃特尔,因在“固体表面的化学反应”研究中取得了开拓性成就而获得诺贝尔化学奖.他的成就之一是证实了氢气与氮气在固体催化剂表面合成氨气的反应过程.如图所示是该反应的模型图 (○表示氢原子,●表示氮原子) 
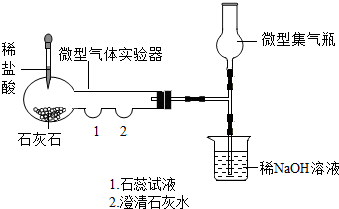 (1)挤压胶头,滴入盐酸.过一会儿,用燃着的木条放在微型集气瓶口,若木条火焰熄灭,则说明二氧化碳已收集满.
(1)挤压胶头,滴入盐酸.过一会儿,用燃着的木条放在微型集气瓶口,若木条火焰熄灭,则说明二氧化碳已收集满.