题目内容
要炼得56t含杂质3%的生铁,需要含Fe2O3 80%的赤铁矿多少吨?
考点:含杂质物质的化学反应的有关计算
专题:有关化学方程式的计算
分析:据56t含杂质3%的生铁,计算出生铁中铁的质量,并据方程式计算需要赤铁矿的质量.
解答:解:56t含杂质3%的生铁中含有铁的质量是:56t×(1-3%)=54.32t
设要炼得56t含杂质3%的生铁,需要含Fe2O3 80%的赤铁矿质量为x
Fe2O3+3CO
2Fe+3CO2
160 112
80%×x 54.32t
=
x=97t
答:要炼得56t含杂质3%的生铁,需要含Fe2O3 80%的赤铁矿97t.
设要炼得56t含杂质3%的生铁,需要含Fe2O3 80%的赤铁矿质量为x
Fe2O3+3CO
| ||
. |
160 112
80%×x 54.32t
| 160 |
| 112 |
| 80%×x |
| 54.32t |
x=97t
答:要炼得56t含杂质3%的生铁,需要含Fe2O3 80%的赤铁矿97t.
点评:明确纯物质的质量=不纯物质的质量×纯物质的质量分数,并熟练书写方程式,以及方程式解题的方法即可顺利解答.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
某物质受热后变为气态,则该变化( )
| A、一定是升华 |
| B、一定是化学变化 |
| C、可能是物理变化,也可能是化学变化 |
| D、以上都不对 |
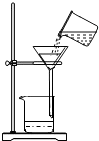 生活离不开水.净化水的知识在日常生活中有着广泛的应用:
生活离不开水.净化水的知识在日常生活中有着广泛的应用: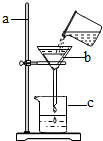 如图是某同学用来除去水中难溶性杂质时所采用的过滤装置图.试回答:
如图是某同学用来除去水中难溶性杂质时所采用的过滤装置图.试回答: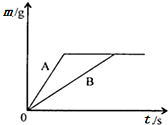 将等质量的锌粉和铁粉,分别放入质量相等、溶质质量分数相同的稀硫酸中,生成氢气质量(m)随反应时间(t)的变化曲线如图所示,请回答下列问题.
将等质量的锌粉和铁粉,分别放入质量相等、溶质质量分数相同的稀硫酸中,生成氢气质量(m)随反应时间(t)的变化曲线如图所示,请回答下列问题.