题目内容
资料表明:在不同温度下,CO可将Fe2O3还原为Fe、Fe3O4中的一种或两种。为探究温度对该反应产物的影响,进行如下实验。
【查阅资料】
Ⅰ.Fe3O4与盐酸反应,得到FeCl2和FeCl3的混合溶液
 Ⅱ.用溶质质量分数一定的FeCl2和FeCl3溶液进行如下实验,为方案设计提供参考
Ⅱ.用溶质质量分数一定的FeCl2和FeCl3溶液进行如下实验,为方案设计提供参考
| FeCl2溶液 | FeCl3溶液 | |
| 加入Fe | 无明显变化 | 溶液变成浅绿色 |
| 加试剂A | 无明显变化 | 溶液变成红色 |
【实验过程】
甲、乙两组同学分别用酒精灯和酒精喷灯作为热源进行CO还原Fe2O3的实验,检验得到的黑色固体的成分,实验记录如下。
| 实验操作 | 实验现象 | 结论与解释 |
| ①取少量的黑色固体于试管中,滴加适量的______ ②向步骤①所得的溶液中,滴加试剂A | 甲组: 固体溶解,无气泡冒出 加试剂A后,溶液变成红色 | 黑色固体的成分是______ 甲组用CO还原Fe2O3反应的化学方程式是______ |
| 乙组: 固体溶解, 加试剂A后,溶液颜色无明显变化 | 黑色固体的成分是Fe |
【实验反思】
(1)结合此次探究活动,你认为下列说法正确的是______(填序号)。
a.温度会影响反应的产物
b.试剂A用于检验FeCl3溶液
c.进行CO还原Fe2O3的实验时,一定要进行尾气处理
d.得到的黑色固体的质量一定小于参加反应的Fe2O3的质量
(2)有人认为乙组的实验结论有欠缺,你是否认同此观点,其理由是
。
 【实验过程】
【实验过程】
①稀盐酸 Fe3O4 CO + 3Fe2O3 2Fe3O4 + CO2 有气泡冒出
【实验反思】
(1)abcd
(2)认同,若固体是Fe和Fe3O4的混合物,过量的Fe可与FeCl3反应生成FeCl2,加入试剂A同样能观察到溶液无明显变化。(2分)

 名校课堂系列答案
名校课堂系列答案水是重要的资源。
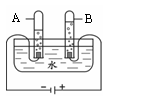
(1)右图为电解水的装置,A试管中的气体是______。通过此实验
证明水是由______组成的。
 | |||
 | |||

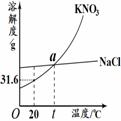
 (2)右图是硝酸钾和氯化钠的溶解度曲线。
(2)右图是硝酸钾和氯化钠的溶解度曲线。
①图中a点表示的含义是  。
。
②20℃,向100 g水中加入50 g KNO3,所得溶液为______
(填“饱和”或“不饱和”)。若要提高该溶液中溶质的质量
分数,其方法是 。
 (3)20℃,按下图实验得到的溶液中,溶质和溶剂的质量比是______。
(3)20℃,按下图实验得到的溶液中,溶质和溶剂的质量比是______。
下列根据实验操作和现象所得出的结论正确的是
| 选项 | 实验操作 | 实验现象 | 结 论 |
| A. | SO2通入酸性高锰酸钾溶液中 | 紫红色褪去 | SO2具有漂白性 |
| B. | 向无色溶液中加硝酸酸化的BaCl2溶液 | 有白色沉淀 | 原溶液中定含SO42- |
| C. | 向Na2SiO3溶液中通入适量CO2气体 | 出现白色沉淀 | H2CO3的酸性比H2SiO3强 |
| D. | 向某溶液中先加氯水再加KSCN溶液 | 溶液呈血红色 | 原溶液中定含Fe2+ |
 B.溶液质量减少
B.溶液质量减少  O的摩尔质量为20 g·mol-1 ( )
O的摩尔质量为20 g·mol-1 ( ) 和S2-具有相同的质子数和电子数 ( )
和S2-具有相同的质子数和电子数 ( )