题目内容
氧化铜,碳粉及不参加反应的杂质组成的混合物8.8g,当隔绝空气加强热后,氧化铜与碳粉刚好完全反应,冷却称的剩余物质质量为6.6g,求反应后生成铜的质量,并求原混合物中杂质的质量分数.(只考虑生成气体为二氧化碳)
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:根据碳粉和氧化铜在高温的条件下会生成铜和二氧化碳,然后结合题中的数据进行解答.
解答:解:设参加反应的氧化铜的质量为x,碳粉质量为y,生成铜的质量为z,
2CuO+C
2Cu+CO2↑ 固体减少
160 12 128 44
x y z (8.8-6.6)g
=
=
=
x=8g,y=0.6g,z=6.4g
所以混合物中杂质为:8.8g-8g-0.6g=0.2g
所以杂质的质量分数为:
×100%=2.3%
答:反应后生成铜的质量是6.4g,原混合物中杂质的质量分数是2.3%.
2CuO+C
| ||
160 12 128 44
x y z (8.8-6.6)g
| 160 |
| x |
| 12 |
| y |
| 128 |
| z |
| 44 |
| (8.8-6.6)g |
x=8g,y=0.6g,z=6.4g
所以混合物中杂质为:8.8g-8g-0.6g=0.2g
所以杂质的质量分数为:
| 0.2g |
| 8.8g |
答:反应后生成铜的质量是6.4g,原混合物中杂质的质量分数是2.3%.
点评:本题难度不大,根据质量守恒定律判断出固体减少的质量是生成二氧化碳的质量是解答本题的突破口.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案
相关题目
诗词是民族灿烂文化中的瑰宝.下列诗句中隐含有化学变化的是( )
| A、千里冰封,万里雪飘 |
| B、只要功夫深,铁杵磨成针 |
| C、野火烧不尽,春风吹又生 |
| D、夜来风雨声,花落知多少 |
下列实验对应的图象正确的是( )
| A | B | C | D |
| 将等质量的镁和锌分别与足量的盐酸反应 | 向pH=2的盐酸中滴加过量的氢氧化钠溶液 | 向盐酸和氯化铁的混合溶液中加入过量的氢氧化钠溶液 | 向pH=12的氢氧化钠溶液中加水稀释 |
 |  |  | 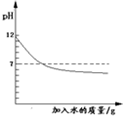 |
| A、A | B、B | C、C | D、D |
下列实验操作正确的是( )
A、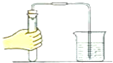 检查气密性 |
B、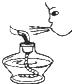 熄灭酒精灯 |
C、 读取液体体积 |
D、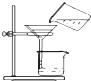 过滤 |
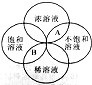 溶液是否饱和与溶液的“浓”“稀”之间没有必然的联系,不能根据溶液的“浓”“稀”来判断溶液是否饱和,只有当溶液、溶质、温度相同时,饱和溶液才一定比不饱和溶液浓.例如20℃时的NaCl饱和溶液比20℃时的NaCl不饱和溶液浓,具体关系可如图所示,则图中有A、B两种情况,请举例说明.
溶液是否饱和与溶液的“浓”“稀”之间没有必然的联系,不能根据溶液的“浓”“稀”来判断溶液是否饱和,只有当溶液、溶质、温度相同时,饱和溶液才一定比不饱和溶液浓.例如20℃时的NaCl饱和溶液比20℃时的NaCl不饱和溶液浓,具体关系可如图所示,则图中有A、B两种情况,请举例说明.