题目内容
1.通过一年的学习,相信你已经初步掌握了实验室制取气体的有关知识.请结合图示回答问题.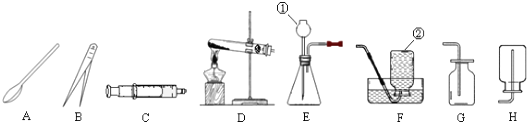
(1)写出图中标示的仪器名称:①长颈漏斗,②集气瓶.
(2)实验室用高锰酸钾制取比较纯净的O2,应选用的装置组合为DF(填字母序号,下同),写出该反应的化学方程式2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(3)实验室用大理石和稀盐酸制取比较干燥的CO2,应选用的装置组合为EG;收集的气体中常含有一些氯化氢气体(HCl),这是由于盐酸具有挥发性.若要验证二氧化碳气体已收集满,其操作是将燃着的木条放在集气瓶口处,火焰熄灭则证明已集满二氧化碳.
分析 (1)熟记仪器的名称;
(2)根据发生装置和收集装置的选择方法、排水法收集和排空气法收集气体的区别、方程式的书写方法考虑;
(3)根据制取二氧化碳的药品、反应条件、气体的性质确定相关装置;根据二氧化碳的性质确定验满方法.
解答 解:(1)①是长颈漏斗、②是集气瓶;故填:长颈漏斗;集气瓶;
(2)高锰酸钾制氧气反应物属于固体需要加热,需要酒精灯,由于氧气不易溶于水可以用排水法收集,密度比空气大可以用向上排空气法收集,因为排水法收集到的气体比排空气法收集到的气体纯净,所以实验室用高锰酸钾制取并收集比较纯净氧气应选用的装置组合是DF;写方程式要注意一写二配三注明四等号.用高锰酸钾制氧气反应物是高锰酸钾,生成物是锰酸钾、二氧化锰和氧气,配平方法是用观察法配平,反应条件是加热写在等号的上边,氧气后面标上上升符号;
故填:DF;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(3)实验室制取二氧化碳的反应物是固体与液体,故选择装置E来制取,二氧化碳的密度比空气大,且能溶于水,所以用G收集;盐酸具有挥发性,所以制取的二氧化碳中混有少量的氯化氢气体;二氧化碳不燃烧、也不支持燃烧,所以验满时,可将燃着的木条放在集气瓶口,观察木条是否熄灭;故填:EG;挥发;将燃着的木条放在集气瓶口处,火焰熄灭则证明已集满二氧化碳.
点评 本考点主要考查气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
相关题目
8.下列四种物质久置空气中,质量增加且没有新物质生成的是( )
| A. | 氨水 | B. | 烧碱 | C. | 浓硫酸 | D. | 浓盐酸 |
12.下列有关化学反应类型的判断,错误的是( )
| A. | SO3+H2O═H2SO4 化合反应 | |
| B. | NH4HCO3═NH3↑+H2O+CO2↑ 分解反应 | |
| C. | 2Al+WO3═Al2O3+W 置换反应 | |
| D. | 6CO2+6H2O$→_{叶绿素}^{光照}$C6H12O6+6O2 复分解反应 |
16.除去下列物质中的少量杂质所用的方法正确的是( )
| 选项 | 物质 | 杂质 | 除去杂质的方法 |
| A | 硫酸钡 | 硫酸铜 | 加足量水溶解、过滤、洗涤、干燥 |
| B | 水 | 臭味物质 | 加入适量活性炭,充分吸附 |
| C | 氢氧化钠溶液 | 氧氧化钙溶液 | 加入适量的碳酸钾溶液,过滤 |
| D | 二氧化碳 | 水蒸气 | 通过盛有足量生石灰的干燥管 |
| A. | A | B. | B | C. | C | D. | D |
6.下列有关物质的提纯、除杂、区分、鉴别所用的试剂或方法错误的是( )
| A. | 从含有少量杂质NaCl的KNO3固体中,提纯KNO3,采用加水溶解、蒸发结晶的方法 | |
| B. | 除去Cu中少量CuO,通过加入稀盐酸溶解、过滤、洗涤、干燥的方法 | |
| C. | 可用水区分NH4NO3和NaOH两种固体 | |
| D. | 仅用组内物质就能鉴别出FeCl3、KOH、MgSO4、KNO3四种溶液 |
11.下列对相应微粒的描述中,不正确的是( )
| A. | 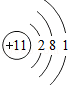 易得电子 | B. | 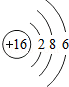 易形成阴离子 | C. |  带负电荷 | D. | 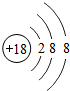 化学性质稳定 |

 A~H是初中化学常见的物质,已知A为黑色固体单质,G为紫红色固体单质,B为红棕色粉末,F为黑色粉末,它们的转化关系如图所示,请回答:
A~H是初中化学常见的物质,已知A为黑色固体单质,G为紫红色固体单质,B为红棕色粉末,F为黑色粉末,它们的转化关系如图所示,请回答: