题目内容
7. 试根据图中信息回答下列问题
试根据图中信息回答下列问题(1)为什么沙漠地区铁制品锈蚀较慢沙漠地区缺水.
(2)用铝来制高压锅说明铝有具有导热性性质.
(3)养鱼池中设立水泵目的是增大水与空气的接触面积,增加水中氧气的溶解量
(4)制面包、糕点的发酵粉中一种物质的俗称是小苏打.
分析 物质的性质决定物质的用途,根据已有的物质的性质进行分析解答即可.
解答 解:(1)铁与氧气和水接触生锈,沙漠地区空气中水蒸气含量少,生锈慢,故填:沙漠地区缺水;
(2)用铝来制高压锅利用的是铝的导热性,故填:导热性;
(3)养鱼池中设立水泵可以增大水与空气的接触面积,增加水中氧气的溶解量,故填:增大水与空气的接触面积,增加水中氧气的溶解量;
(4)制面包、糕点的发酵粉中含有小苏打碳酸氢钠,故填:小苏打.
点评 本题考查的是常见的物质的用途,完成此题可以依据物质的性质进行.

练习册系列答案
 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案
相关题目
17.下列对于氢氧化钠溶液样品是否变质进行的相关实验中,实验现象及结论合理的是( )
| A. | 取少量溶液样品,滴入酚酞试液,酚酞变红,说明没有变质 | |
| B. | 若样品部分变质,滴入稀盐酸,立即有大量气体产生 | |
| C. | 取一定量溶液样品,滴入适量的澄清石灰水,过滤,向滤液中滴加酚酞溶液,溶液变红,证明原样品中含有氢氧化钠 | |
| D. | 向溶液样品中加入适量的澄清石灰水至恰好完全反应,过滤,可除去样品中的杂质 |
18.下列操作或现象与分子的特性对应错误的选项是( )
| 选项 | 操作或现象 | 分子的特性 |
| A | 给篮球充气 | 分子间有间隔 |
| B | 在花园中可闻到花的香味 | 分子的不断运动 |
| C | 100mL酒精和100mL水混合在一起,体积小于200mL | 分子的体积变小 |
| D | 加热氧化汞可得到金属汞和氧气 | 在化学变化中分子是可以再分的 |
| A. | A | B. | B | C. | C | D. | D |
2.生活处处有化学,有关下列说法不正确的是( )
| A. | 医疗上的生理盐水是用氯化钠配制的 | |
| B. | 碳酸钙可用作补钙剂 | |
| C. | 碳酸钠用于肥皂,石油,造纸纺织和印染等工业 | |
| D. | 农业上用石灰乳和硫酸铜等配制成具有杀菌作用的波尔多液 |
12.实验室常用的干燥剂“碱石灰”是CaO和NaOH固体的混合物.同学们为确认一瓶久置的“碱石灰”样品的成分,进行如下实验探究.
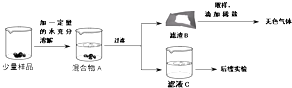
滤渣B中一定含有CaCO3,产生该物质的化学方程式可能是Ca(OH)2+Na2CO3=CaCO3↓+2NaOH滤液C成分的探究.
【猜想】滤液C中的溶质可能为①NaOH;②Na2CO3;③NaOH和Na2CO3;④NaOH和Ca(OH)2
【设计方案并进行实验】甲、乙同学分别设计如下方案并进行探究:
甲同学:取滤液C少许放入试管中,滴加足量的稀盐酸,产生大量无色气体,则滤液C中的溶质是Na2CO3.
乙同学:取滤液C少许放入试管中,滴加一定量的无色酚酞,液体变成红色,则滤液C中的溶质一定含有NaOH.
【反思与评价】丙同学认真分析上述两位同学的实验,认为他们的结论均有不足之处,请说出丙认为甲、乙同学不足之处的理由甲同学:加入足量盐酸,产生大量气体,可能有氢氧化钠被消耗后与碳酸钠溶液反应;
乙同学:实验中加无色酚酞溶液,变红则滤液中还可能有碳酸钠,碳酸钠溶液也能使酚酞变红;为进一步确认猜想③正确,请你帮助他设计实验进行验证.
实验过程中,同学们还发现向样品中加入一定量水溶解时放出大量的热并综合对滤液和滤渣成分的探究,下列对样品成分的分析正确的是②③(填序号).①样品中一定含NaOH ②样品中一定含Na2CO3
③样品中含NaOH、CaO中的一种或两种.

滤渣B中一定含有CaCO3,产生该物质的化学方程式可能是Ca(OH)2+Na2CO3=CaCO3↓+2NaOH滤液C成分的探究.
【猜想】滤液C中的溶质可能为①NaOH;②Na2CO3;③NaOH和Na2CO3;④NaOH和Ca(OH)2
【设计方案并进行实验】甲、乙同学分别设计如下方案并进行探究:
甲同学:取滤液C少许放入试管中,滴加足量的稀盐酸,产生大量无色气体,则滤液C中的溶质是Na2CO3.
乙同学:取滤液C少许放入试管中,滴加一定量的无色酚酞,液体变成红色,则滤液C中的溶质一定含有NaOH.
【反思与评价】丙同学认真分析上述两位同学的实验,认为他们的结论均有不足之处,请说出丙认为甲、乙同学不足之处的理由甲同学:加入足量盐酸,产生大量气体,可能有氢氧化钠被消耗后与碳酸钠溶液反应;
乙同学:实验中加无色酚酞溶液,变红则滤液中还可能有碳酸钠,碳酸钠溶液也能使酚酞变红;为进一步确认猜想③正确,请你帮助他设计实验进行验证.
| 实验操作 | 实验现象 | 实验结论 |
| 取少量滤液C于试管中取少量滤液C于试管中,加入足量CaCl2溶液,过滤,在滤液中滴加无色酚酞试液 | 有白色沉淀生成,溶液由无色变成红色 | 猜想③正确 |
③样品中含NaOH、CaO中的一种或两种.
19.下列实验基本操作或仪器的使用中没有错误的是( )
| A. | 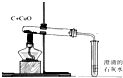 木炭还原氧化铜 | B. |  过滤 | C. |  蒸发 | D. | 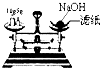 称取氯化钠固体 |
16.下表列出的是生活和工业中常用的三种漂白剂.
(1)上述漂白剂中,Ca(ClO)2属于②(填序号).①混合物 ②化合物 ③氧化物
(2)ClO2中氯元素的化合价为+4.
(3)次氯酸钙〔Ca(ClO)2〕是漂白粉的有效成分.
①次氯酸钙在潮湿的空气中久置会生成具有漂白性的物质次氯酸(HClO)和难溶于水的白色固体,反应的化学方程式Ca(ClO)2+H2O+CO2═CaCO3↓+2HClO.
②工业使用漂白粉时常根据(3)中①的反应原理,通过添加少量的B (填序号)物质来解决漂白粉漂白缓慢的问题
A.氢氧化钠 B.稀盐酸 C.氢氧化钙 D.氯化钠.
| 种类 | 亚氯 酸钠 | 二氧 化氯 | 漂白粉 |
| 化学 式 | NaClO2 | ClO2 | Ca(ClO)2和 CaCl2 |
(2)ClO2中氯元素的化合价为+4.
(3)次氯酸钙〔Ca(ClO)2〕是漂白粉的有效成分.
①次氯酸钙在潮湿的空气中久置会生成具有漂白性的物质次氯酸(HClO)和难溶于水的白色固体,反应的化学方程式Ca(ClO)2+H2O+CO2═CaCO3↓+2HClO.
②工业使用漂白粉时常根据(3)中①的反应原理,通过添加少量的B (填序号)物质来解决漂白粉漂白缓慢的问题
A.氢氧化钠 B.稀盐酸 C.氢氧化钙 D.氯化钠.
 农业技术的发展使越来越多的新鲜蔬菜水果走进人们的生活.请回答:
农业技术的发展使越来越多的新鲜蔬菜水果走进人们的生活.请回答: