题目内容
17.生活中处处有化学.很多食品中放有干燥剂,就是利用其具有吸收水分的功能,生石灰就是一种.请写出生石灰吸收水分的化学方程式CaO+H2O═Ca(OH)2,该反应属于反应放热(填“放热”或“吸热”).分析 根据生石灰与水反应生成氢氧化钙解答;
解答 解:生石灰与空气中的水反应生成氢氧化钙,反应的化学方程式为:CaO+H2O═Ca(OH)2,该反应属于放热反应,故生石灰需要密封保存.
答案:CaO+H2O═Ca(OH)2;放热;
点评 本题是对常见的碱的性质的考查,解题的关键是对两种常见的碱的性质的了解,属基础性知识考查题.

练习册系列答案
 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案
相关题目
5.健康是人生的主题.下列与人体健康有关的叙述正确的是( )
①喝牛奶、豆浆等富含蛋白质的食品可有效缓解煤气中毒
②人体胃液的pH为0.9~1.5
③人体摄入过量的氟元素可导致龋齿
④人体中的酶都是在体温和中性条件下进行催化的.
①喝牛奶、豆浆等富含蛋白质的食品可有效缓解煤气中毒
②人体胃液的pH为0.9~1.5
③人体摄入过量的氟元素可导致龋齿
④人体中的酶都是在体温和中性条件下进行催化的.
| A. | ①②③④ | B. | ②③④ | C. | ②④ | D. | ② |
12.下列各组物质按单质、氧化物、混合物的顺序排列的是( )
| A. | 冰、干冰、赤铁矿 | B. | 氢气、生石灰、煤 | ||
| C. | 红磷、纯碱、石油 | D. | 金刚石、熟石灰、空气 |
10.铁与水蒸气能发生反应生成一种常见铁的氧化物和一种气体.某化学学习小组的同学对此反应很感兴趣,在小组集体协作下设计了如图实验,以探究铁粉与水蒸气反应后的产物,也邀请你一起来完成下列探究:
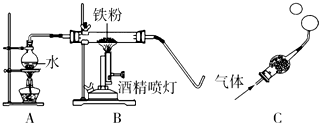
(1)A装置的作用是 ①提供水蒸气.
(2)探究生成的气体是什么?
【猜想与假设】猜想一:生成的气体可能是氢气;猜想二:生成的气体可能是氧气.
【实验探究】将生成的气体通入球形管里装有碱石灰干燥剂.导管口蘸些肥皂水(或洗涤剂溶液),控制气体流速,吹出肥皂泡.当肥皂泡吹到一定大时,轻轻摆动导管,肥皂泡脱离管口后,气泡上升.用燃着的木条靠近肥皂泡,有爆鸣声.
【推断】生成的气体是②氢气.
(3)探究试管中剩余固体成分是什么?
【查阅资料】
【初步验证】试管中剩余固体为黑色,能全部被磁铁吸引.
【猜想与假设】猜想一:剩余固体是Fe和Fe3O4;猜想二:剩余固体是 ③Fe3O4.
【实验探究】
【实验结论】铁与水蒸气反应的化学方程式为:⑥3Fe+4H2O$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2.
【反思与交流】该黑色固体不可能是FeO、Fe2O3,理由是 ⑦FeO不能被磁铁吸引,Fe2O3红棕色粉末且不能被磁铁吸引.

(1)A装置的作用是 ①提供水蒸气.
(2)探究生成的气体是什么?
【猜想与假设】猜想一:生成的气体可能是氢气;猜想二:生成的气体可能是氧气.
【实验探究】将生成的气体通入球形管里装有碱石灰干燥剂.导管口蘸些肥皂水(或洗涤剂溶液),控制气体流速,吹出肥皂泡.当肥皂泡吹到一定大时,轻轻摆动导管,肥皂泡脱离管口后,气泡上升.用燃着的木条靠近肥皂泡,有爆鸣声.
【推断】生成的气体是②氢气.
(3)探究试管中剩余固体成分是什么?
【查阅资料】
| 常见铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
| 颜色、状态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
| 能否被磁铁吸引 | 否 | 否 | 能 |
| 能否与盐酸反应 | 能 | 能 | 能 |
【猜想与假设】猜想一:剩余固体是Fe和Fe3O4;猜想二:剩余固体是 ③Fe3O4.
【实验探究】
| 实验操作 | 实验现象及结论 |
| ④取少量黑色固体于试管中,加入足量的稀盐酸 | ⑤若固体全部溶解,没有气泡冒出,则猜想二正确;若固体全部溶解,有气泡冒出,则猜想一正确 |
【反思与交流】该黑色固体不可能是FeO、Fe2O3,理由是 ⑦FeO不能被磁铁吸引,Fe2O3红棕色粉末且不能被磁铁吸引.
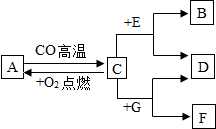 现有A、B、C、D、E、F、G七种物质,C、F是最常见的金属,B是气体单质,D为FeSO4溶液,G为CuSO4溶液,它们之间存在如图所示关系:
现有A、B、C、D、E、F、G七种物质,C、F是最常见的金属,B是气体单质,D为FeSO4溶液,G为CuSO4溶液,它们之间存在如图所示关系: