题目内容
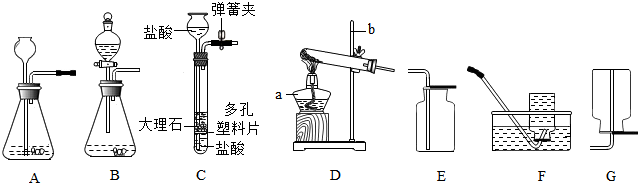
16. 某化学小组用一定量AgNO3和Al(NO3)3的混合溶液进行了如图实验,已知溶液甲呈蓝色.
某化学小组用一定量AgNO3和Al(NO3)3的混合溶液进行了如图实验,已知溶液甲呈蓝色.(1)Ag、Al、Cu、Zn四种金属的金属活动性由强到弱的顺序为Al、Zn、Cu、Ag;
(2)向固体乙上滴加盐酸时,没有(填“有”或“没有”)气泡产生;
(3)溶液甲中一定含有哪些溶质?Al(NO3)3、Zn(NO3)2、Cu(NO3)2.(写化学式)
分析 根据在金属活动性顺序中,Al>Zn>H>Cu>Ag,氢前的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,据此分析回答有关的问题.
解答 解:在金属活动性顺序中,Al>Zn>H>Cu>Ag,向一定量AgNO3和Al(NO3)3的混合溶液加入铜粉和锌粉的混合物,锌与先硝酸银反应生成硝酸锌和银,当锌粉完全反应,铜再与硝酸银反应产生硝酸铜和银,而铝的活动性最强,所以不能发生反应.由于过滤后滤液中呈蓝色,说明了溶液中有硝酸铜,锌完全参加了反应,铜与硝酸银发生了反应.
(1)由上述分析可知,Ag、Al、Cu、Zn四种金属的活动性由强到弱的顺序为:Al>Zn>H>Cu>Ag;
(2)因为有硝酸铜的存在,因此就不会有比铜活动性强的锌剩余,因此过滤、洗涤后往固体乙中加入稀盐酸,无气泡产生;
(3)溶液甲中含有没参加反应的硝酸铝,反应产生的硝酸锌,硝酸铜,所以溶液甲中一定含有溶质的化学式是:Al( NO3) 3、Zn( NO3)2、Cu(NO3 ) 2.
故答案为:(1)Al>Zn>H>Cu>Ag;(2)没有;(3)Al( NO3) 3、Zn( NO3)2、Cu(NO3 ) 2.
点评 本题考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序的意义结合题目的信息分析滤液和滤渣的成分.

练习册系列答案
 智慧小复习系列答案
智慧小复习系列答案
相关题目
7.空气中含量较多且能用于医疗急救的气体是( )
| A. | 氧气 | B. | 氮气 | C. | 二氧化碳 | D. | 惰性气体 |
1.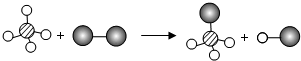 已知某两种物质在光照条件下能发生化学反应,其微观示意图如图:(说明:一种小球代表一种元素的原子)则下列说法正确的是( )
已知某两种物质在光照条件下能发生化学反应,其微观示意图如图:(说明:一种小球代表一种元素的原子)则下列说法正确的是( )
 已知某两种物质在光照条件下能发生化学反应,其微观示意图如图:(说明:一种小球代表一种元素的原子)则下列说法正确的是( )
已知某两种物质在光照条件下能发生化学反应,其微观示意图如图:(说明:一种小球代表一种元素的原子)则下列说法正确的是( )| A. | 该反应属于置换反应 | B. | 图示中的反应物都是单质 | ||
| C. | 图示中共有4种分子 | D. | 该图示不符合质量守恒定律 |
6.节能减排,保护环境,是我们共同点责任.下列做法与此倡导不相符的是( )
| A. | 家庭中,提倡垃圾分离 | B. | 工作中,采取无纸化办公 | ||
| C. | 工业上,回收废旧金属再利用 | D. | 交通上,拓宽马路,鼓励私家车出行 |


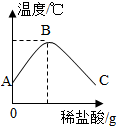 将稀盐酸慢慢滴入盛有氢氧化钠溶液的烧杯中,用温度计测量烧杯中溶液的温度,温度随加入稀盐酸的质量变化曲线如图所示:
将稀盐酸慢慢滴入盛有氢氧化钠溶液的烧杯中,用温度计测量烧杯中溶液的温度,温度随加入稀盐酸的质量变化曲线如图所示: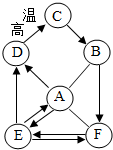 A、B、C、D、E、F均为初中化学中常见的物质,E俗称纯碱,它们之间存在如图的转化关系.“→”表示物质间存在着相应的转化关系,“-”表示物质间能发生反应(部分反应物、生成物和反应条件未标出).
A、B、C、D、E、F均为初中化学中常见的物质,E俗称纯碱,它们之间存在如图的转化关系.“→”表示物质间存在着相应的转化关系,“-”表示物质间能发生反应(部分反应物、生成物和反应条件未标出).