题目内容
10.青少年一定要爱护自己的眼睛,在光线不足时看书、写字要用照明工具,如图是一种照明用台灯.
(1)如图中标示的各部件中,用金属材料制成的是①②④(填序号).
(2)灯管后面的反光片为铝箔,铝块能制成铝箔是利用了铝的延展性.铝制品具有很好的抗腐蚀性,原因是4Al+3O2═2Al2O3(用化学方程式解释).
(3)若要验证铜、铁、铝的活动性顺序,某同学已经选择了打磨过的铜片和铝片,你认为他还需要的一种溶液是硫酸亚铁(填溶质的化学式).
(4)废弃的电器需分类回收,请简述废旧金属回收的意义是可节约金属资源.
分析 (1)根据金属材料包括金属单质及合金,从中找出金属材料;
(2)利用金属的延展性可把金属压成片、拉成丝;通常情况下,铝能和空气中的氧气反应生成一层致密的氧化铝薄膜;
(3)若要验证三种金属的活动性,如果只用一种溶液,就要选择活动性居中的金属的盐溶液;
(4)根据节约金属资源的意义进行分析解答.
解答 解:(1)金属单质及合金都属于金属材料,①铁螺丝钉、②铝箔反光片、④铜质插头都属于金属材料;故答案为:①②④;
(2)利用金属铝具有良好的延展性可把金属铝制成片;铝制品具有很好的抗腐蚀性能,其原因是铝能和氧气反应生成氧化铝保护膜,反应的化学方程式为:4Al+3O2═2Al2O3;故答案为:延展;4Al+3O2═2Al2O3;
(3)验证三种金属的活动性,如果只用一种溶液,就要选择活动性居中的金属的盐溶液,又因为根据金属活动性顺序,铜、铁、铝三种金属中铁的活动性居中,所以应选用硫酸亚铁溶液或者氯化亚铁溶液.故答案为:硫酸亚铁;
(4)回收废旧金属,可节约金属资源;可节约能源;降低金属制品的生产成本;可减少金属对环境的污染,故填:可节约金属资源.
点评 本题综合考查了金属的性质、金属活动性顺序以及回收金属的知识,都是初中化学重点学习的内容.

练习册系列答案
相关题目
13.以淀粉、二氧化硅(SiO2)为载体,吸附酒精制作而成的现代新型食品保鲜剂.保鲜原理是酒精缓慢挥发,在食品周围形成一定浓度的气体保护层.下列说法不正确的是( )
| A. | 作为载体的淀粉和SiO2具有吸附性 | |
| B. | 气体保护层是利用了酒精的杀菌作用 | |
| C. | 酒精挥发时分子间隔变大 | |
| D. | 该保鲜剂能与明火接触 |
14.某地成功处置了一辆满载三氯化磷(PCl3)的车辆泄漏事故.三氯化磷是一种重要的无极工业产品,无色液体、密度1.574g/cm3 (21℃),熔点-112℃,沸点75.5℃,易燃.遇水反应生成亚磷酸(H3PO3)和氯化氢,与有机物接触会着火.下列对三氯化磷的说法错误的是( )
| A. | H3PO3中磷元素的化合价为+3 | |
| B. | 运输途中应防雨淋和防高温 | |
| C. | 运输过程中如果发生燃烧时,可以用水浇灭 | |
| D. | 三氯化磷与水反应的化学方程式:PCl3+3H2O═H3PO3+3HCl↑ |
15.如图实验方案的设计中,没有正确体现对比这种科学思想的是( )
| A. | 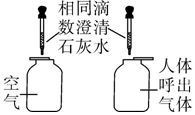 比较二氧化碳的含量 | B. | 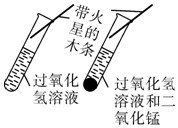 研究二氧化锰的催化作用 | ||
| C. | 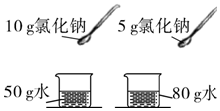 配制氯化钠溶液 | D. |  区分硬水和软水 |
2.下列各组物质分别置于密闭容器中,在一定条件下充分反应后,密闭容器中的气态物质肯定为纯净物的是( )
| A. | 分子数比为1:1的H2和O2 | B. | 质量比为3:8的C和O2 | ||
| C. | 质量比为1:5的CH4和O2 | D. | 分子数比为1:1的CO和O2 |
19.艾草中含有的黄酮素(C15H11O2)有很高的药用价值,关于黄酮素的说法正确的是( )
| A. | 是一种有机化合物 | |
| B. | 氧元素的质量分数最大 | |
| C. | 由27个原子构成 | |
| D. | 碳、氢、氧三种元素的质量比为15:11:2 |
20.制取氧气是初中化学重要的实验之一,兴趣小组进行如下探究.
探究一 氧气的制取

(1)a仪器名称:长颈漏斗;C图操作的名称:检查装置气密性.
(2)用氯酸钾制取氧气选择的发生装置是B(填序号).
写出该反应的化学方程式2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
探究二 催化剂的选择
研究表明,许多金属氧化物对氯酸钾有催化作用,分别用下列金属氧化物作催化剂,氯酸钾开始发生分解反应和反应剧烈时的温度如表所示:
(3)上述实验中,从温度对反应催化效果来看,最好选用氧化铜作催化剂.
(4)加热氢氧化铜固体可制得氧化铜和一种常见液体物质,写出该反应的化学方程式Cu(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CuO+H2O.
探究三 氧化铜与二氧化锰的催化效果进行比较
用如图装置进行实验,实验均以生成25mL气体为准,可能影响实验的因素均以忽略,相关装置和数据见下表:
(5)实验①的作用对比,上述实验中的“待测数据”是收集25mL氧气所需时间,若b>c,(填“>”、“=”或“<”)可知在某温度下氧化铜对氯酸钾分解效果更好.
探究一 氧气的制取

(1)a仪器名称:长颈漏斗;C图操作的名称:检查装置气密性.
(2)用氯酸钾制取氧气选择的发生装置是B(填序号).
写出该反应的化学方程式2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
探究二 催化剂的选择
研究表明,许多金属氧化物对氯酸钾有催化作用,分别用下列金属氧化物作催化剂,氯酸钾开始发生分解反应和反应剧烈时的温度如表所示:
| 温度/℃ | Fe2O3 | Al2O3 | CuO | MgO |
| 开始反应 | 470 | 515 | 305 | 490 |
| 剧烈反应 | 490 | 540 | 350 | 545 |
(4)加热氢氧化铜固体可制得氧化铜和一种常见液体物质,写出该反应的化学方程式Cu(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CuO+H2O.
探究三 氧化铜与二氧化锰的催化效果进行比较
用如图装置进行实验,实验均以生成25mL气体为准,可能影响实验的因素均以忽略,相关装置和数据见下表:
| 序号 | KClO3质量 | 催化剂质量 | 待测数据 |
| ① | 2.45g | - | a |
| ② | 2.45g | 0.51gMnO2 | b |
| ③ | 2.45g | 0.51gCuO | c |