题目内容
14. 把某稀硫酸分为等体积的两份,放入两个烧杯中,分别加入等质量的甲、乙两种金属,反应后金属都没有剩余.产生H2的质量随时间变化的趋势如图.下列说法正确的是( )
把某稀硫酸分为等体积的两份,放入两个烧杯中,分别加入等质量的甲、乙两种金属,反应后金属都没有剩余.产生H2的质量随时间变化的趋势如图.下列说法正确的是( )| A. | 反应消耗等质量的金属 | B. | 甲的活动性比乙强 | ||
| C. | 反应消耗等质量的硫酸 | D. | 甲的相对原子质量一定比乙小 |
分析 等质量的甲、乙两种金属,反应后金属都没有剩余,说明酸是足量的,金属反应完全时乙用的时间少反应速度快,活动性较强,生成氢气量的不同决定了甲乙的相对原子质量的高低,利用这些知识可解决此题.
解答 解:A、放入的金属质量相等,反应后均无剩余,所以反应消耗等质量的金属,故A说法正确;
B、由图象可知,反应完全时乙用的时间少,反应速度快,活动性较强,即乙的活动性比甲强,故B说法错误;
C、生成氢气量的不同,说明消耗酸的质量不同,因为氢气来源于酸中的氢,故C说法错误;
D、根据金属与酸反应时,一定量金属完全反应产生氢气质量=$\frac{金属元素化合价}{金属的相对原子质量}$×金属的质量,所以甲的相对原子质量不一定比乙小,如铝和镁,故D说法错误
故选:A.
点评 此题是一道图象分析题,解题的关键是读懂图象,并能找到与图象结合的信息,属基础型常规考查题.

练习册系列答案
相关题目
2.下列有关物质的分类,错误的是( )
| A. | 甲烷属于有机物 | B. | 水属于氧化物 | C. | 氧气属于纯净物 | D. | 空气属于化合物 |
9.根据下表信息,完成表中空格:
| 化学符号 | $\stackrel{+2}{Ca}$Cl2 | Fe2+ | 3N2 | 2SO42- |
| 符号的意义 | 氯化钙中钙元素为+2价 | 亚铁离子 | 3个氮气分子 | 2个硫酸根离子 |

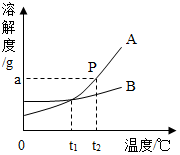 小刚同学绘制了如图所示A、B两种固体物质的溶解度曲线.
小刚同学绘制了如图所示A、B两种固体物质的溶解度曲线.