题目内容
4.高氯酸钠晶体(NaClO4•H2O)可用于制备高氯酸.粗盐除去泥沙等不容性杂质后得到“精盐”(只含MgCl2、CaCl2两种杂质),以“精盐”为原料制备高氯酸钠晶体的流程如下:【资料】高氯酸钠在较高温度下容易分解.
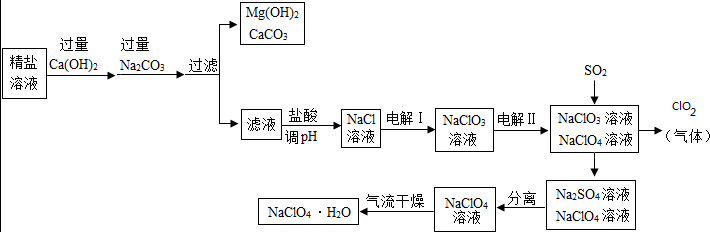
请回答下列问题:
(1)滤液中溶质除NaCl外还含有NaOH、Na2CO3.
(2)ClO2中氧元素的化合价是-2.
(3)通入SO2是为了除去NaClO4溶液中少量的NaClO3,该反应的化学方程式为SO2+2NaClO3=Na2SO4+2ClO2.
(4)“气流干燥”时温度应控制在75°C~95°C之间,其原因是温度过高,高氯酸钠晶体失去结晶水或高氯酸钠分解,温度过低,干燥不充分.
分析 (1)根据加入过量的碳酸钠来分析;
(2)根据化合物中氧元素的化合价来分析;
(3)根据化学方程式的书写方法来分析;
(4)根据高氯酸钠的性质来分析.
解答 解:(1)粗盐溶液中加入过量的氢氧化钙是为了除净镁离子,加入过量的碳酸钠,是为了除净钙离子,此时滤液中有氯化钠还是剩余的碳酸钠;故填:NaOH、Na2CO3;
(2)ClO2中氧元素的化合价是-2价;故填:-2;
(3)二氧化硫与氯酸钠反应生成硫酸钠和二氧化氯,故填:SO2+2NaClO3=Na2SO4+2ClO2;
(4)因为高氯酸钠在较高温度下容易分解或失去结晶水,温度过低,干燥不充分;所以“气流干燥”时温度应控制在75°C~95°C之间,故填:温度过高,高氯酸钠晶体失去结晶水或高氯酸钠分解,温度过低,干燥不充分.
点评 本题考查物质的制备实验的工业设计,题目难度中等,本题注意把握物质的性质,为解答该题的关键.

练习册系列答案
 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目
14.关于水的说法正确的是( )
| A. | 水是人体必需的营养素之一 | B. | 可用煮沸方法检验软水和硬水 | ||
| C. | 生活污水可直接排放到江河中 | D. | 电解水时电源负极产生氧气 |
15.下列有关化学史的叙述错误的是( )
| A. | 我国化学家侯德榜在工业制烧碱的研究中取得了巨大成就 | |
| B. | 拉瓦锡得出了空气是由氧气和氮气组成的结论 | |
| C. | 汤姆森发现了电子,证实原子是可分的 | |
| D. | 俄国化学家门捷列夫将当时已发现的63种元素排序,制得了第一张元素周期表 |
12.把少量下列物质分别放入水中,充分搅拌,可以得到溶液的是( )
| A. | 豆油 | B. | 蔗糖 | C. | 面粉 | D. | 泥土 |
19.只用下列鉴别方法不能把待鉴别物质区分开的是( )
| 选项 | 待鉴别物质 | 鉴别方法 |
| A | 软水、硬水 | 分别滴加肥皂水,搅拌,观察产生泡沫多少 |
| B | 棉纤维、羊毛纤维 | 分别点燃,闻燃烧产生的气味 |
| C | 氯化钠溶液、稀盐酸 | 分别滴加酚酞溶液,观察溶液颜色变化 |
| D | 氯化钾溶液、硫酸钠溶液 | 分别滴加氢氧化钡溶液,观察现象 |
| A. | A | B. | B | C. | C | D. | D |
8.下列图象不能正确反映其对应操作的是( )
| A. | 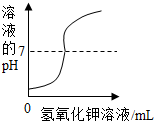 向一定量的稀硫酸中逐滴滴入氢氧化钾溶液 向一定量的稀硫酸中逐滴滴入氢氧化钾溶液 | |
| B. |  等质量的Zn和Mg分别与等体积等质量分数的稀硫酸(足量)反应 等质量的Zn和Mg分别与等体积等质量分数的稀硫酸(足量)反应 | |
| C. | 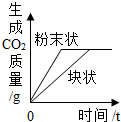 等质量CaCO3分别与等体积等质量分数的稀盐酸(足量)反应 等质量CaCO3分别与等体积等质量分数的稀盐酸(足量)反应 | |
| D. | 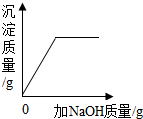 向硫酸和硫酸铜混合溶液加入氢氧化钠 向硫酸和硫酸铜混合溶液加入氢氧化钠 |