题目内容
5.请根据如图所示的实验过程和提供的数据完成下列计算: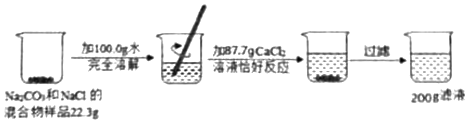
(1)生成沉淀的质量为10g.
(2)实验室用20g溶质质量分数为20%氯化钙溶液,水、氯化钙固体,配得上述所需溶液,所需氯化钙固体的质量为11.1g.
(3)通过计算,求出滤液中溶质的质量分数.
分析 碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,根据反应的化学方程式及其提供的数据可以进行相关方面的计算和判断.
解答 解:(1)生成沉淀的质量为:22.3g+100.0g+87.7g-200g=10g.
故填:10.
(2)设碳酸钠质量为x,氯化钙质量为y,生成氯化钠质量为z,
Na2CO3+CaCl2═CaCO3↓+2NaCl,
106 111 100 117
x y 10g z
$\frac{106}{x}$=$\frac{111}{y}$=$\frac{100}{10g}$=$\frac{117}{z}$,
x=10.6g,y=11.1g,z=11.7g,
配得上述所需溶液,所需氯化钙固体的质量为11.1g.
(3)滤液中溶质的质量分数为:$\frac{22.3g-10.6g+11.7g}{200g}$×100%=11.7%,
答:滤液中溶质的质量分数是11.7%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案
相关题目
15.下列物质在氧气中燃烧的主要现象的叙述正确的是( )
| A. | 硫在氧气中燃烧,生成无色.无味的二氧化硫气体 | |
| B. | 木炭在氧气中燃烧生成无色的二氧化碳 | |
| C. | 磷在氧气中燃烧生成的白雾是五氧化磷 | |
| D. | 铁丝在氧气中燃烧,火星四射,生成黑色固体物质 |
13.将一定质量的a、b、c、d四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得反应后各物质的质量如下,下列说法中错误的是( )
| 物质 | a | b | c | d |
| 反应前质量(g) | 6.4 | 3.2 | 4.0 | 0.5 |
| 反应后质量(g) | 待测 | 2.56 | 7.2 | 0.5 |
| A. | a和b是反应物,d一定是催化剂 | |
| B. | 反应后a物质的质量为4.64g | |
| C. | 若物质a与b的相对分子质量之比为2:1,则反应中a与b的化学计量数之比为2:1 | |
| D. | c物质中元素的种类,一定等于a、b二种物质中元素的种类 |
17.铜锈的主要成分是碱式碳酸铜.碱式碳酸铜受热分解的化学方程式为:Cu2(OH)2CO3=2CuO+X+CO2↑下列说法正确的是( )
| A. | 反应前后固体物质中铜元素的质量分数不变 | |
| B. | X是相对分子质量最小的氧化物 | |
| C. | 反应前后铜元素的化合价发生了改变 | |
| D. | 加热Cu2(OH)2CO3的实验装置和实验室制取CO2的发生装置相同 |
15.逻辑推理是一种重要的化学思维方法.下列推理合理的是( )
| A. | 因为碱溶液呈碱性,所以呈碱性的溶液一定是碱溶液 | |
| B. | 因为氧化物含有氧元素,所以含氧元素的化合物都是氧化物 | |
| C. | 因为H2O和H2O2的组成元素相同,所以它们的化学性质相同 | |
| D. | 因为蜡烛燃烧生成CO2和H2O,所以蜡烛组成里一定含有碳元素和氢元素 |
 2008年5月12日,我国汶川发生大地震.全国人民“众志成城,抗震救灾”.
2008年5月12日,我国汶川发生大地震.全国人民“众志成城,抗震救灾”. 某中学综合实践活动小组在进行“诚信商品”研究时,检验商品标签所列成分及其含量与实际是否相符.随机取出市售某“纯碱”样品(成分说明见下图),经检验杂质仅是氯化钠.准确称取样品10.9g,加入150克氯化钙溶液后恰好完全反应,将反应生成的沉淀物经过滤、洗涤、烘干,得到白色固体10g.
某中学综合实践活动小组在进行“诚信商品”研究时,检验商品标签所列成分及其含量与实际是否相符.随机取出市售某“纯碱”样品(成分说明见下图),经检验杂质仅是氯化钠.准确称取样品10.9g,加入150克氯化钙溶液后恰好完全反应,将反应生成的沉淀物经过滤、洗涤、烘干,得到白色固体10g.