题目内容
实验室探究氧气的性质需要一定质量的氧气。我校一化学兴趣小组为了探究氧气的性质需,用托盘天平准确称取3.16g高锰酸钾装入试管连接装置,加热制取和收集氧气,待高锰酸钾完全反应后,称剩余固体物质的质量为2.84g。请你参与计算:
(1)在锰酸钾中钾元素和锰元素的质量比为 ;
(2)3.16g高锰酸钾完全反应后,收集的氧气的质量为 (理论值,不计损失);
(3)在剩余固体物质中,由于锰酸钾能溶于水,二氧化锰不溶于水,可用溶解、过滤、烘干的方法获得纯净的二氧化锰,作为氯酸钾或过氧化氢溶液分解的催化剂。在上述反应中,最多可回收多少二氧化锰?
(1) 78:55(1分)(2)0.32g(1分)
 (3)[解]设:最多可回收MnO2的质量为x。 (0.5分)
(3)[解]设:最多可回收MnO2的质量为x。 (0.5分)
2KMnO4 K2MnO4+ MnO2 + O2↑ (1分)
87 32
X 0.32g (1分)
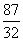
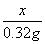
== (1分)
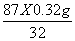

x === ===0.87g (1分)
32g
答:最多可回收MnO2的质量为0.87g。 (0.5分)
(解答过程合理即可)

CO、CO2和N2的混合气体120g,其中碳元素的质量分数为20%.使该混合气体与足量的灼热氧化铁完全反应,再将气体通入过量的澄清石灰水中,充分反应后得到白色沉淀的质量为( )
|
| A. | 50g | B. | 100g | C. | 150g | D. | 200g |
下列物质在空气中最不容易燃烧的是( )
|
| A. | 铁片 | B. | 镁条 | C. | 木炭 | D. | 氢气 |
人体结石有多种,其中一种含有较多的草酸钙(CaC2O4),CaC2O4中碳元素的化合价是( )
|
| A. | +1 | B. | +2 | C. | +3 | D. | +4 |
在地壳中含量最多的金属元素是( )
|
| A. | O | B. | Si | C. | Al | D. | Fe |
 H4 D.SiF4
H4 D.SiF4  某研究性小组的同学对沙坪坝区内某地水质状况进行调查研究,将取得的水样进行
某研究性小组的同学对沙坪坝区内某地水质状况进行调查研究,将取得的水样进行