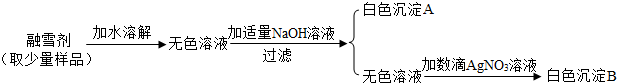
题目内容
20. 小明在化学实验室看到一瓶硝酸钾固体,瓶上标签的部分内容如图所示.
小明在化学实验室看到一瓶硝酸钾固体,瓶上标签的部分内容如图所示.(1)用化学用语填空:
硝酸钾中含有的离子是K+和NO3-,在农业生产上可以为农作物提供的营养元素是N,标出KNO3中氮元素的化合价H$\stackrel{+5}{N}$O3.
(2)硝酸钾中钾、氮、氧三种元素的质量比是39:14:48,其中氮元素的质量分数为13.9%(精确到0.1%).
分析 (1)本题考查化学用语的意义及书写,解题关键是分清化学用语所表达的对象是分子、原子、离子还是化合价,才能在化学符号前或其它位置加上适当的计量数来完整地表达其意义,并能根据物质化学式的书写规则正确书写物质的化学式,才能熟练准确的解答此类题目.
(2)根据元素质量比=相对原子质量与相应原子个数的乘积比计算分析;
根据化合物中元素的质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%,进行分析
解答 解:(1)硝酸钾中含有的离子是K+和硝酸根离子,根据离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.硝酸根离子是由多个原子组成的离子,整体带1个单元位的负电荷,表示为NO3-;
在农业生产上可以为农作物提供的营养元素是氮元素,其符号为:N;
元素化合价的表示方法:确定出化合物中所要标出的元素的化合价,然后在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,所以标出KNO3中氮元素的化合价,故可表示为:H$\stackrel{+5}{N}$O3;
(2)元素的质量比等于元素相对原子质量和的比,KNO3中钾、氮、氧元素的质量比
为=39:14:16×3=39:14:48;
(3)KNO3中氮元素的质量分数=$\frac{14}{101}$×100%≈13.9%,
故答案为:(1)NO3-;N;H$\stackrel{+5}{N}$O3;(2)39:14:48;13.9%
点评 此题是对硝酸钾的相关知识的考查,解决的重点是掌握有关硝酸钾化学式的计算,属基础性知识考查题.

练习册系列答案
相关题目
10.请设计简单的实验方案(步骤、现象、结论)
| 实验目的 | 实验步骤 | 实验现象及结论 |
| 探究:分解过氧化氢制氧气反应中二氧化锰作用 | ①在试管中加少量一定浓度过氧化氢溶液,稍后将带火星木条伸入试管; ②向上试管中加入少量二氧化锰,将带火星木条伸入试管; ③上试管中无现象时,重新加H2O2液,将带火星木条伸入试管,再重复上述操作 | 木条不复燃,产生气体少; 产生气泡,木条复燃,产生氧气多; 木条复燃,二氧化锰的量无变化,反应中起催化作用. |
8.逻辑推理是一种重要的化学思维方法,以下推理合理的是( )
| A. | 碱性溶液能使酚酞试液变红,滴入酚酞试液后变红的溶液一定呈碱性 | |
| B. | 锌和铜均是金属,锌与稀硫酸反应生成氢气,则铜也能与稀硫酸反应生成氢气 | |
| C. | 酸能使石蕊试液变红,CO2也能使紫色的石蕊试液变红,所以CO2是酸 | |
| D. | 化合物都是由不同元素组成的,不同元素组成的物质一定是化合物 |
5.下列物质中,前者属于纯净物,后者属于混合物的是( )
| A. | 碳酸饮料 氧气 | B. | 二氧化碳 干净的河水 | ||
| C. | 氮气 红磷 | D. | 矿泉水 白酒 |
12.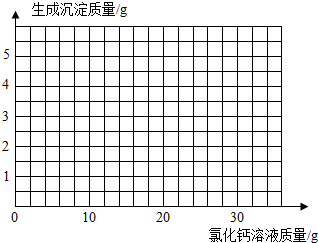 课外活动小组的同学在测定由NaCl和Na2C03形成的固体混合物组成时,进行了以下实验:取40g固体混合物配成溶液,平均分为四份,然后分别加入一定质量分数的CaCl2溶液,实验数据见下表:
课外活动小组的同学在测定由NaCl和Na2C03形成的固体混合物组成时,进行了以下实验:取40g固体混合物配成溶液,平均分为四份,然后分别加入一定质量分数的CaCl2溶液,实验数据见下表:
请分析表中数据回答并计算
(1)m=4g.
(2)求原固体混合物中Na2CO3的质量分数.
(3)求CaCl2溶液的溶质质量分数.
(4)请在图中画出在10g固体混合物中加入CaCl2溶液的质量与产生沉淀质量变化关系的示意图.
 课外活动小组的同学在测定由NaCl和Na2C03形成的固体混合物组成时,进行了以下实验:取40g固体混合物配成溶液,平均分为四份,然后分别加入一定质量分数的CaCl2溶液,实验数据见下表:
课外活动小组的同学在测定由NaCl和Na2C03形成的固体混合物组成时,进行了以下实验:取40g固体混合物配成溶液,平均分为四份,然后分别加入一定质量分数的CaCl2溶液,实验数据见下表:| 实验一 | 实验二 | 实验三 | 实验四 | |
| 原固体混合物质量 | 10g | 10g | 10g | 10g |
| 加入CaCl2溶液质量 | 10g | 20g | 30g | 40g |
| 生成沉淀的质量 | 2g | m | 5g | 5g |
(1)m=4g.
(2)求原固体混合物中Na2CO3的质量分数.
(3)求CaCl2溶液的溶质质量分数.
(4)请在图中画出在10g固体混合物中加入CaCl2溶液的质量与产生沉淀质量变化关系的示意图.
9.根据如图的信息判断,下列关于铝的说法错误的是( )


| A. | 在化学反应中,原子易失去电子形成Al3+ | |
| B. | 核电荷数是10 | |
| C. | 相对原子质量是26.982 | |
| D. | 属于金属元素 |