题目内容
18.用如图甲所示装置制二氧化碳并进行二氧化碳与过氧化钠(Na2O2)的反应.资料:过氧化钠(Na2O2)是一种淡黄色固体,能与CO2,H2O发生反应:
Na2O2+2CO2→2Na2CO3+O2,2Na2O2+H2O→4NaOH+O2↑
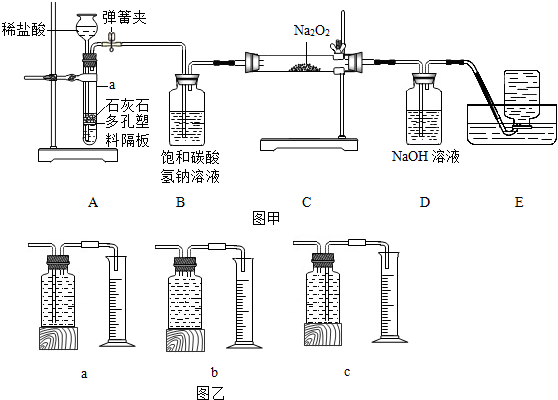
①写出仪器a的名称试管.
②装置A中发生反应的化学方程式为CaCO3+2HCl=CaCl2+CO2↑+H2O,利用装置A制取CO2的优点是随开随用,随关随停.
③装置B的作用是吸收CO2中混有的HCl,装置D的作用是除去二氧化碳气体.
④装置E中收集到的气体是O2(填化学式),该气体还可以用图乙中的c进行收集(填写字母序号).
⑤为探究反应后装置C中固体的成分,甲同学取固体于试管中,加足量水,无气泡产生,则固体中一定没有过氧化钠.将所得溶液分成两份,进行下表所示实验:
| 实验操作 | 实验现象 | 分析与结论 |
| 向一份溶液中滴加稀盐酸 | 有气泡产生 | C中固体有碳酸钠 |
| 向另一份溶液中滴加加入过量氯化钙溶液后滴入无色酚酞试液 | 变红 | C中固体有氢氧化钠 |
分析 ①据常用仪器的名称解答;
②据二氧化碳的制取原理,不同的实验装置,功能不同解答;
③根据氢氧化钠和二氧化碳反应生成碳酸钠和水进行分析;
(4)根据过氧化钠和二氧化碳、水反应会生成氧气,氢氧化钠可以将二氧化碳除去进行分析;
(5)根据过氧化钠和水会生成氧气,碳酸钠和氯化钙会生成碳酸钙沉淀,碳酸钙和盐酸反应会生成二氧化碳气体,氢氧化钠溶液显碱性进行分析④⑤
解答 解:①写出仪器a的名称是试管;
②二氧化碳的实验室制法是用稀盐酸与大理石(或石灰石.其主要成分都是碳酸钙)反应来制取.其反应原理是CaCO3+2HCl=CaCl2+CO2↑+H2O;实验室制二氧化碳时,A装置的优点是随开随用,随关随停;
③氢氧化钠和二氧化碳反应生成碳酸钠和水,所以装置D的作用是除去二氧化碳气体;
④过氧化钠和二氧化碳、水反应会生成氧气,氢氧化钠可以将二氧化碳除去,所以装置E中收集到的气体是O2,氧气密度比空气大,不易溶于水,密度比水小,所以还可以用下列图2装置中的c进行收集;
(5)过氧化钠和水会生成氧气,碳酸钠和氯化钙会生成碳酸钙沉淀,碳酸钙和盐酸反应会生成二氧化碳气体,碱能使无色的酚酞试液变红色.
固体加水没有气泡,所以不含过氧化钠,加入盐酸,会生成气体,所以含有碳酸钠;向另一份溶液中加入过量氯化钙溶液后滴入无色酚酞试液,酚酞变红,则说明有氢氧化钠存在.
故答案为:①试管; ②CaCO3+2HCl=CaCl2+CO2↑+H2O、随开随用,随关随停; ③除去二氧化碳气体; ④O2、c;⑤过氧化钠;稀盐酸;加入过量氯化钙溶液后滴入无色酚酞试液;变红.
点评 解答此题的关键是根据反应物的类型及反应条件正确选择装置,正确进行知识的类比和前后联系,熟知典型的化学方程式的书写.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
6.既具有可燃性又具有还原性的氧化物是( )
| A. | CO | B. | CH4 | C. | H2 | D. | CO2 |
13.除去物质中的杂质(括号内是杂质),操作正确的是( )
| 选项 | 物质 | 操作方法 |
| A | C(CuO) | 通入足量的H2,加热 |
| B | NaCl溶液(Na2CO3) | 加入适量的Ca(NO3)2溶液,充分反应后过滤 |
| C | NaOH溶液(Ca(OH)2) | 通入过量CO2气体,充分反应后过滤 |
| D | CuSO4溶液(H2SO4) | 加入过量CuO粉末,加热,充分反应后过滤 |
| A. | A | B. | B | C. | C | D. | D |
9.美国洛斯-阿拉莫斯国家实验室的研究人员日前用普通水制造出了一种新型的固体物质.科学家介绍说,这种新型固体物质的分子中仅包含有一个氢原子和一个氧原子.下列说法正确的是( )
| A. | 该物质和水是同种物质 | |
| B. | 该物质属于新型化合物 | |
| C. | 该物质中氢元素与氧元素的质量比为1:1 | |
| D. | 普通水制成该物质后,分子停止运动 |
 海水中蕴含含有80多种元素,海洋是一座巨大的宝库.氯碱工业以海水为原材料可以大量制取烧碱和氧气,它们都是重要的化工生产原料,可以进一步加工成多种化工产品,广泛用于工业生产.所以氯碱工业及相关产品几乎涉及国民经济及人民生活的各个领域.
海水中蕴含含有80多种元素,海洋是一座巨大的宝库.氯碱工业以海水为原材料可以大量制取烧碱和氧气,它们都是重要的化工生产原料,可以进一步加工成多种化工产品,广泛用于工业生产.所以氯碱工业及相关产品几乎涉及国民经济及人民生活的各个领域.