题目内容
7.无色混合气体可能存在水蒸气、一氧化碳、二氧化碳、氯化氢和氢气,将气体通过浓硫酸,气体体积没有变化,再通过澄清石灰水后,没有出现浑浊,但气体体积缩小一半,尾气导出后能燃烧,燃绕后产生的气体能使无水硫酸铜变蓝,却不能使澄清石灰水变浑浊,则该气体中一定存在HCl、H2,肯定不存在(填分子式)H2O、CO,写出发生反应的化学方程式为:Ca(OH)2+2HCl═CaCl2+2H2O,CaCO3+HCl=CaCl2+H2O+CO2↑,2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2.分析 几种气体都是无色气体,通过浓硫酸后气体体积没有变化,则肯定没有水蒸气,再通过澄清石灰水后,也没有出现浑浊变化,但气体体积减少一半,则没有二氧化碳,含有氯化氢气体,点燃导出的尾气,燃绕后产生的气体能使无水硫酸铜变蓝,却不能使澄清石灰水变浑浊,则燃烧产物有水,没有二氧化碳,则原混合气体中没有氢气,含有一氧化碳.
根据题干提供的信息结合物质的性质进行分析,(1)将混合气体通过浓硫酸后,气体体积没有变化,浓硫酸具有的是吸水性,说明气体中没有水蒸气;
(2)再通过澄清石灰水后,没有发现浑浊现象,但气体体积缩小一半,说明有能与氢氧化钙反应的物质存在,可以是氯化氢气体,也可能是氯化氢和二氧化碳的混合气体,故一定含有氯化氢,可能含有二氧化碳;
(3)点燃导出的尾气,燃绕后产生的气体能使无水硫酸铜变蓝,却不能使澄清石灰水变浑浊,则燃烧产物有水,没有二氧化碳,则原混合气体中没有氢气,含有一氧化碳.
解答 解:(1)将混合气体通过浓硫酸后,气体体积没有变化,浓硫酸具有的是吸水性,说明气体中没有水蒸气.
(2)再通过澄清石灰水后,没有发现浑浊现象,但气体体积缩小一半,说明有能与氢氧化钙反应的物质存在,可以是氯化氢气体,也可能是氯化氢和二氧化碳的混合气体,故一定含有氯化氢,可能含有二氧化碳.
(3)点燃导出的尾气,燃绕后产生的气体能使无水硫酸铜变蓝,却不能使澄清石灰水变浑浊,则燃烧产物有水,没有二氧化碳,则原混合气体中没有氢气,含有一氧化碳.综上所述,该混合气体中一定含有氯化氢和氢气,一定没有水蒸气和一氧化碳,可能含有二氧化碳.
故答案为:
HCl、H2,H2O、CO;Ca(OH)2+2HCl═CaCl2+2H2O、CaCO3+HCl=CaCl2+H2O+CO2↑、2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2
点评 学生能利用物质的性质或特性来确定混合物中的成分,则应注意在学习过程中多积累有关物质检验的方法.

 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案| A. | 镁+氧气$\stackrel{点燃}{→}$氧化镁 | B. | 甲烷+氧气$\stackrel{点燃}{→}$二氧化碳+水 | ||
| C. | 碳酸氢铵$\stackrel{加热}{→}$氨气+二氧化碳+水 | D. | 硫+氧气$\stackrel{点燃}{→}$二氧化硫 |
| A. | 燃烧需要同时满足三个条件,所以灭火也要同时控制这三个条件 | |
| B. | 溶液具有均一性和稳定性,所以具有均一性、稳定性的液体一定是溶液 | |
| C. | 活泼金属与稀盐酸反应放出气体,所以与稀盐酸反应放出气体的物质一定是活泼金属 | |
| D. | 某物质充分燃烧生成二氧化碳和水,所以该物质的组成里一定含有碳、氢两种元素 |
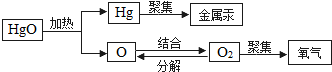 化学是在原子、分子水平上研究物质及其变化的科学.
化学是在原子、分子水平上研究物质及其变化的科学.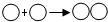 表示氧分子的形成过程
表示氧分子的形成过程